Dysprosium(III)-oxid
chemische Verbindung
From Wikipedia, the free encyclopedia
Dysprosium(III)-oxid ist eine chemische Verbindung aus der Gruppe der Oxide.

| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
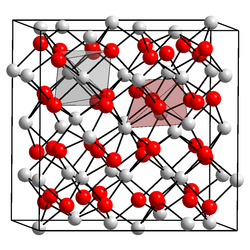 | ||||||||||||||||
| _ Dy3+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Dysprosium(III)-oxid | |||||||||||||||
| Andere Namen |
Dysprosia | |||||||||||||||
| Verhältnisformel | Dy2O3 | |||||||||||||||
| Kurzbeschreibung |
weißes, leicht hygroskopisches Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 373,00 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Dichte |
7,81 g·cm−3 (25 °C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
3900 °C[3] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,9757[5] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Geschichte
Im Jahr 1878 wurden Erbiumerze entdeckt, die neben diesem auch Holmium- und Thulium(III)-oxid enthielten. Der französische Chemiker Paul Émile Lecoq de Boisbaudran konnte während der Arbeit mit Holmium(III)-oxid im Jahre 1886 in Paris noch Dysprosium(III)-oxid isolieren und entdeckte damit das Element Dysprosium.[6]
Gewinnung und Darstellung
Dysprosium(III)-oxid kann durch Verbrennung von Dysprosium an Luft gewonnen werden.[7]
Eigenschaften
Verwendung
Dysprosium(III)-oxid wird für spezielle Zwecke in Glas, Leuchtstoffen, Lasern und Halogen-Metalldampflampen eingesetzt. Es wird weiterhin in Cermets für Kernreaktor-Steuerstäbe verwendet.[1] Als Dotierungsmittel für Bariumtitanat-Kondensatoren wird es für kleine Kondensatoren hoher Kapazität eingesetzt.[10] Aufgrund seiner magnetischen Eigenschaften ist es für Motoren und Generatoren interessant.[11]

