Flavin-Adenin-Dinukleotid
Coenzym, phosphorylierte organische Verbindung
From Wikipedia, the free encyclopedia
Flavin-Adenin-Dinukleotid, abgekürzt FAD ist ein Coenzym. Es hat eine wichtige Bedeutung als Elektronenüberträger in verschiedenen prokaryotischen und eukaryotischen Stoffwechselprozessen, wie der oxidativen Phosphorylierung[4], der β-Oxidation von Fettsäuren, der Atmungskette und anderen Redoxreaktionen.[5] FAD kann im Gegensatz zum NAD+ einzelne Elektronen übertragen.[5] Oxidoreduktasen können somit mittels FAD molekularen Sauerstoff aktivieren.[6]

| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
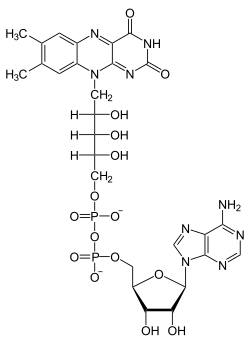 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Flavin-Adenin-Dinukleotid | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C27H33N9O15P2 | |||||||||||||||||||||
| Kurzbeschreibung |
gelber Feststoff[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 785,55 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Löslichkeit |
löslich in Wasser[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Struktur und chemische Eigenschaften
FAD besteht aus Adenosindiphosphat, das mit Riboflavin (Vitamin B2) verknüpft ist. Alternativ könnte man auch sagen, es bestehe aus Adenosin-Monophosphat (AMP), an welchem Flavinmononukleotid (FMN) gebunden ist. Die „reaktiven“ Stickstoffatome befinden sich im Isoalloxazinring des Moleküls.
Das oxidierte FAD geht durch Aufnahme zweier Protonen (H+) und zweier Elektronen (e−) in die reduzierte Form FADH2 über:[2] Man bezeichnet dies als einen ECEC-Mechanismus (e für elektrochemischer Schritt, c für chemischer Schritt der Protonierung), wobei die zweite Protonierung nur in ausreichend saurer Lösung erfolgt. Der Übergang zwischen dem ECE-Mechanismus ohne abschließende Übertragung eines Protons und des ECEC-Mechanismus ist außerdem noch von der chemischen Umgebung abhängig: Für freies FAD in Lösung überlappen ECE- und ECEC-Mechanismus bei pH 6,7[7], auf Oberflächen immobilisiertes FAD wird erst bei etwa pH 9 nach dem ECE-Mechanismus reduziert.[8]
Das Redoxpotential des FAD liegt unter Standardbedingungen bei −219 mV vs. NHE.[7]

Eine Lösung von Flavin-Adenin-Dinukleotid in Wasser (10 g·l−1) besitzt einen pH-Wert von etwa 6.
Enzyme, die FAD verwenden
Zu den Enzymen, die FAD verwenden, gehören die:
- Monoamin-Oxidase
- Ferredoxin-NADP+ Reduktase
- Glucose-Oxidase (GOx)
- Cellobiose Dehydrogenase
- Nitratreduktase
- Succinat-Dehydrogenase
- Dihydrolipoyl-Dehydrogenase
- Acyl-CoA-Dehydrogenase