Niob(V)-chlorid
chemische Verbindung
From Wikipedia, the free encyclopedia
Niob(V)-chlorid ist eine salzartige chemische Verbindung bestehend aus den Elementen Niob und Chlor.

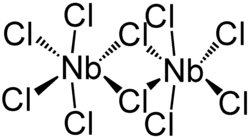
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Niob(V)-chlorid | ||||||||||||||||||
| Andere Namen |
Niobpentachlorid | ||||||||||||||||||
| Summenformel | NbCl5 | ||||||||||||||||||
| Kurzbeschreibung |
gelber Feststoff mit stechendem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 270,17 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
2,75 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
248,2 °C[1] | ||||||||||||||||||
| Löslichkeit |
heftige Zersetzung in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Gewinnung und Darstellung
Niob(V)-chlorid kann durch Reaktion von Niob mit Chlor gewonnen werden.[2]
Ebenfalls möglich ist Darstellung durch Reaktion von Niob(V)-oxid mit Thionylchlorid oder Kohlenstofftetrachlorid[2] oder Hexachlorpropen[3]:
Eigenschaften

Es handelt sich um einen gelben Feststoff mit stechendem Geruch (Bildung von Chlorwasserstoff durch Hydrolyse), der sich heftig in Wasser zersetzt.
Niob(V)-chlorid bildet eine dimere Struktur aus, bei welcher jedes Niobatom sechsfach durch Chloro-Liganden koordiniert ist. Zwei Chloratome fungieren als Brückenliganden. Es existieren zwei kristalline Polymorphe von Niob(V)-chlorid; in beiden wird eine verzerrt-oktaedrische Struktur ausgebildet, bei der die pseudo-axialen Chloroliganden in einem Winkel von ca. 84 ° zur pseudo-equatorialen Ebene angeordnet sind.[4][5]
Verwendung
Niob(V)-chlorid wird in der organischen Chemie als Lewis-Säure verwendet. So findet es beispielsweise in der Aktivierung von Alkenen in der Carbonyl-En-Reaktion Anwendung.[6]






![{\displaystyle {\mathrm {Nb} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{5}}{}+{}5\,\mathrm {CCl} {\vphantom {A}}_{\smash[{t}]{2}}{=}\mathrm {CClCCl} {\vphantom {A}}_{\smash[{t}]{3}}{}\mathrel {\longrightarrow } {}2\,\mathrm {NbCl} {\vphantom {A}}_{\smash[{t}]{5}}{}+{}5\,\mathrm {CCl} {\vphantom {A}}_{\smash[{t}]{2}}{=}\mathrm {CClCOCl} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/9224e29e3fbeca822582f6d89a921f2a11ac91d9)