Samarium(III)-oxid
chemische Verbindung
From Wikipedia, the free encyclopedia
Samarium(III)-oxid ist eine chemische Verbindung aus der Gruppe der Oxide.

| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
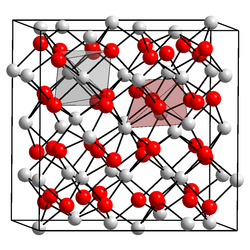 | ||||||||||||||||
| _ Sm3+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Samarium(III)-oxid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | Sm2O3 | |||||||||||||||
| Kurzbeschreibung |
geruchloser gelblicher Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 348,72 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
8,347 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser (20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Geschichte
Samarium(III)-oxid wurde 1879 von Paul Émile Lecoq de Boisbaudran im Samarskit entdeckt.[3]
Gewinnung und Darstellung
Samarium(III)-oxid kann durch Verbrennung von Samarium an Luft gewonnen werden.
Es kann auch durch thermische Zersetzung von Samariumsalzen wie Samariumoxalat oder Samariumcarbonat bei Temperaturen um 700 °C gewonnen werden.[4]
Samarium(III)-oxid-Nanopartikel können durch Reaktion von Samariumhydrid mit Sauerstoff gewonnen werden.[5]
Insgesamt werden etwa 700 Tonnen pro Jahr hergestellt.[6]



