Gliceraldehído-3-fosfato deshidrogenasa
From Wikipedia, the free encyclopedia
La Gliceraldehído-3-fosfato deshidrogenasa (GAPDH) (número EC 1.2.1.12) es una enzima implicada en una de las reacciones más importantes de la glucólisis ruta de Embden-Meyerhof, puesto que cataliza un paso en el cual se genera el primer intermediario de elevada energía, y, además, genera un par de equivalentes de reducción (en forma de NADH). La reacción global es:
- D-gliceraldehído-3-fosfato + NAD+ +Pi <--> 1,3-bisfosfoglicerato + NADH + H+

externos
ExPASy: NiceZime view
KEGG: entrada en KEEG
PRIAM: perfil PRIAM
ExplorEnz: entrada en ExplorEnz
MetaCyc: vía metabólica
| Gliceraldehído-3-fosfato deshidrogenasa | ||||
|---|---|---|---|---|
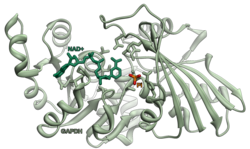 | ||||
| Estructuras disponibles | ||||
| PDB | Buscar ortólogos: PDBe, RCSB | |||
| Identificadores | ||||
| Nomenclatura |
Otros nombres GAPDH, GAPD, G3PD, HEL-S-162eP,
| |||
| Símbolos | GAPDH (HGNC: 4141) GAPD | |||
| Identificadores externos |
ExPASy: NiceZime view KEGG: entrada en KEEG PRIAM: perfil PRIAM ExplorEnz: entrada en ExplorEnz MetaCyc: vía metabólica | |||
| Número EC | 1.2.1.12 | |||
| Locus | Cr. 12 p13.31 | |||
| Ortólogos | ||||
| Especies |
| |||
| Entrez |
| |||
| UniProt |
| |||
| RefSeq (ARNm) |
| |||
| PubMed (Búsqueda) |
| |||
| PMC (Búsqueda) |
| |||

Químicamente, la reacción implica la oxidación del carbonilo del gliceraldehído-3-fosfato hasta un carboxilo, lo que es exergónico en condiciones estándar; en la reacción in vivo, en la que se aprovecha esta energía para generar un compuesto de alta energía, en cambio, la reacción es ligeramente endergónica, pues parte de esta energía queda almacenada en un grupo acil-fosfato, o anhídrido de ácido carboxílico-fosfórico, que posee una energía libre estándar de hidrólisis de ΔG0 = -49,4 kJ/mol. Además, la enzima requiere el coenzima NAD+ a fin de rescatar los electrones producto de la oxidación del sustrato.
Referencias
- Mathews, C. K.; Van Holde, K.E et Ahern, K.G (2003). Bioquímica (3 edición). ISBN 84-7892-053-2.
"esto esta hecho por programadores"

