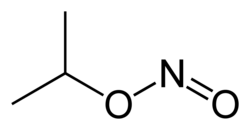
Nitrite d'isopropyle
From Wikipedia, the free encyclopedia
| Nitrite d'isopropyle | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| DCI | Nitrite d'isopropyle | |
| Nom UICPA | Nitrite de 1-méthyléthyle | |
| Synonymes |
Nitrite de 2-propyle |
|
| No CAS | ||
| No ECHA | 100.007.982 | |
| No CE | 208-779-0 | |
| PubChem | 10929 | |
| SMILES | ||
| InChI | ||
| Apparence | liquide huileux jaune clair, d'odeur caractéristique[1][source insuffisante]. | |
| Propriétés chimiques | ||
| Formule | C3H7NO2 [Isomères] |
|
| Masse molaire[2] | 89,093 2 ± 0,003 7 g/mol C 40,44 %, H 7,92 %, N 15,72 %, O 35,92 %, |
|
| Propriétés physiques | ||
| T° ébullition | 40,0 °C[3],[4] | |
| Solubilité | dans l'eau : nulle[réf. nécessaire] | |
| Masse volumique | 0,868 4 g·cm-3[réf. nécessaire] | |
| Précautions | ||
| SGH[3] | ||
| H225, H301, H311, H314, H315, H317, H318, H319, H330, H335, H341, P201, P202, P210, P233, P240, P241, P242, P243, P260, P261 et P264 P270, P271, P272, P280, P281, P284, P310, P312, P320, P321, P322, P330, P361, P362, P363, P301+P310, P301+P330+P331, P302+P352, P303+P361+P353, P304+P340, P305+P351+P338, P308+P313, P332+P313, P333+P313, P337+P313, P370+P378, P405, P403+P233, P403+P235 et P501 |
||
| Écotoxicologie | ||
| CL50 | 2 800 mg/m3 (souris, inhalation)[4] 1 250 mg/m3/4 h (rat, inhalation)[4] |
|
| Caractère psychotrope | ||
| Catégorie | Dépresseur faible | |
| Mode de consommation |
Inhalation des vapeurs |
|
| Autres dénominations |
Voir Poppers |
|
| Risque de dépendance | réputé faible | |
| Composés apparentés | ||
| Autres composés | ||
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Le nitrite d'isopropyle (IPN) ou « nitrite de 2-propyle » désigne un composé chimique synthétique de la famille des nitrites d'alkyle, de formule C3H7ONO. C'est un ester de l'acide nitreux et de l'isopropanol.
Il est hautement toxique (potentiellement mortel) si ingéré, mais ce produit, d'abord mis sur le marché comme médicament, a ensuite été détourné pour d'autres usages : il est depuis les années 1970 utilisé comme drogue récréative (inhalation de sa vapeur utilisée comme « popper », qui lorsqu’il est inhalé détend les muscles lisses des sphincters, donne une impression (éphémère) d’euphorie, génère une sensation de chaleur corporelle et facilite la pénétration anale, ce qui l’a fait apprécier dans certains contextes festifs et/ou sexuels (il est vendu dans les sex-shops sous le nom de poppers).
A température ambiante il se présente comme un liquide huileux jaune pâle, à l'odeur "chimique" caractéristique, et très volatil.
Histoire
Cette famille de composés chimiques a commencé à être synthétisée avant le milieu du XIXe siècle, par Antoine Balard. Les effets de leur inhalation à petites doses ont commencé à être décrits vers la fin des années 1850[5] et Thomas L Brunton l'utilise dans le traitement des affections cardiaques peu après[6], dont l'angine de poitrine[7].
Ce produit a largement remplacé le nitrite d'isobutyle dans les poppers depuis que ce dernier a été déclaré cancérigène et il a les mêmes propriétés de vasodilatateur, mais semble présenter une toxicité intrinsèque pour l’œil et la vision.
Fabrication
Cette molécule est fabriquée à partir d'isopropanol.




