Bariumchromat
chemische Verbindung
From Wikipedia, the free encyclopedia
Bariumchromat ist ein Bariumsalz der Chromsäure. Es besitzt die Formel BaCrO4 und gehört zu Stoffgruppe der Chromate.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
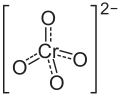 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bariumchromat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | BaCrO4 | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 253,32 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[2] | ||||||||||||||||||
| Dichte |
4,5 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt |
210 °C[2] | ||||||||||||||||||
| Löslichkeit |
sehr schwer in Wasser (0,34 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
0,5 mg·m−3 Barium[4] | ||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Vorkommen

Als natürliche Mineralbildung wurde Bariumchromat erstmals in der Lisdan-Siwaga Falte im Daba-Siwaqa-Komplex innerhalb der Region Hashem des jordanischen Gouvernement Amman entdeckt und von Phoebe L. Hauff, Eugene E. Foord, Sam Rosenblum und Walid Hakki erstbeschrieben.[5] Das Mineral wurde 1978 von der International Mineralogical Association unter dem Namen Hashemit (IMA 1978-006) anerkannt.[6]
Gewinnung/Darstellung
Eigenschaften

Bariumchromat ist ein gelber Feststoff, der praktisch wasserunlöslich und deswegen im Gegensatz zu den meisten anderen Chromaten nicht akut giftig ist, so dass die Sicherheitshinweise für lösliche Chromate für Bariumchromat nur eingeschränkt gelten. Andererseits sind gerade schwerlösliche Chromatpartikel im Falle inhalatorischer Exposition besonders stark karzinogen und Bariumchromat zeigt eine Klastogenwirkung, die über die klassischen genotoxischen Wirkungen löslicher Chrom(VI)-Verbindungen hinausgeht.[7] Wie alle Chromate wirkt auch Bariumchromat oxidierend, besonders stark unter sauren Bedingungen. Es zeigt die für Barium typische grüne Flammenfärbung.
Beim Erhitzen mit Bariumcarbonat wird das sechswertige Chrom zum fünfwertigen reduziert, es bildet sich Bariumchromat(V) Ba3(CrO4)2.[8]
Verwendung
Bariumchromat wird in der Glas- und Farbenindustrie als Pigment eingesetzt. In der Pyrotechnik wird Bariumchromat als Oxidationsmittel und zur Grünfärbung verwendet.




