Bromethanole
Gruppe chemischer Verbindungen
From Wikipedia, the free encyclopedia
Bromethanole ist der Sammelbegriff für organische chemische Verbindungen, die sich vom Ethanol ableiten, wobei ein oder mehrere Wasserstoffatome durch Bromatome ersetzt sind.
| Bromethanole | |||||||||
| Name | 1-Bromethanol | 2-Bromethanol | 2,2-Dibromethanol | 2,2,2-Tribromethanol | |||||
| Andere Namen | Ethylenbromhydrin | Avertin | |||||||
| Strukturformel | 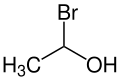 |  |  | ||||||
| CAS-Nummer | 162854-32-2 | 540-51-2 | 83206-47-7 | 75-80-9 | |||||
| PubChem | 14202443 | 10898 | 123582 | 6400 | |||||
| Wikidata | Q82439191 | Q26841231 | Q83113257 | Q25105561 | |||||
| Summenformel | C2H5BrO | C2H4Br2O | C2H3Br3O | ||||||
| Molare Masse | 124,97 g·mol−1 | 203,86 g·mol−1 | 282,76 g·mol−1 | ||||||
| Aggregatzustand | flüssig | fest | |||||||
| Beschreibung | braune klare Flüssigkeit[1] | farblose Flüssigkeit[2] | weiße Kristalle[3] | ||||||
| Schmelzpunkt | −80 °C[4] | 73–79 °C[5] | |||||||
| Siedepunkt | 149–150 °C[4] 56–57 °C (27 hPa)[1] |
179–181 °C[2] | 92–93 °C (13 hPa)[5] | ||||||
| Dichte | 1,763 g·cm−3 (25 °C)[1] | 2,35 g·cm−3 (0 °C)[2] | |||||||
| Dampfdruck | 2,4 mmHg (20 °C)[1] | ||||||||
| Löslichkeit | löslich in Wasser[6] | ||||||||
| Brechungsindex | 1,492[1] | ||||||||
| GHS- Kennzeichnung |
|
|
|
| |||||
| H- und P-Sätze | siehe oben | 301+311+331‐314 | siehe oben | 302‐315‐319‐335 | |||||
| siehe oben | keine EUH-Sätze | siehe oben | keine EUH-Sätze | ||||||
| siehe oben | 261‐280‐301+310‐305+351+338‐310 | siehe oben | 261‐305+351+338 | ||||||
| LD50 | 930 mg/kg (oral, Maus)[5] | ||||||||
Darstellung
Bromethanol
2-Bromethanol kann aus Ethylenoxid und Bromwasserstoff hergestellt werden.[8]

Auch aus Ethylenglycol und Bromwasserstoff oder Phosphortribromid ist die Synthese möglich.[2]

Auch durch Addition von Hypobromiger Säure (HOBr) an Ethylen entsteht 2-Bromethanol.[8] HOBr kann in situ hergestellt, wenn Ethylen in wässriger Lösung mit Brom reagiert.[9]

Dibromethanol
2,2-Dibromethanol entsteht durch Addition von Hypobromiger Säure an Bromethen.[2]

Ferner entsteht es als Nebenprodukt bei der Bromierung von Ethen in wässriger Lösung.[10]

Tribromethanol
2,2,2-Tribromethanol wird durch Reaktion von Aluminiumtriethanolat und elementarem Brom hergestellt.[11]
Eigenschaften
Bromethanol
Aus 2-Bromethanol und Kaliumhydroxid bildet sich durch eine intramolekulare Kondensationsreaktion Ethylenoxid.[2]
Mit Bromwasserstoff reagiert es zu 1,2-Dibromethan weiter.
Dibromethanol
Aus 2,2-Dibromethanol entsteht durch Wasserabspaltung 1,1-Dibromethen.[12]
Mit Kaliumhydroxid entsteht 2-Bromoxiran.[2]
Verwendung
Bromethanol
2-Bromethanol wird bei organischen Synthesen als Reagens genutzt, wenn Carbonsäuregruppen als 2-Bromethylester geschützt werden sollen.[4]
Tribromethanol
Tribromethanol wird unter dem Namen Avertin als Anästhetikum in der Kleintierheilkunde, vor allem bei Mäusen, eingesetzt.[3]







