Caesiumhydroxid
chemische Verbindung
From Wikipedia, the free encyclopedia
Caesiumhydroxid, CsOH, ist das Hydroxid des Caesiums. Es ist in wässriger Lösung eine der stärksten Basen.

| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
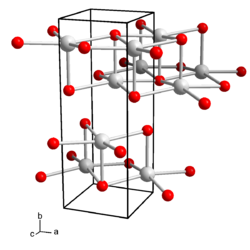 | |||||||||||||||||||
| _ Cs+ _ OH− | |||||||||||||||||||
| Kristallsystem |
orthorhombisch | ||||||||||||||||||
| Raumgruppe |
Cmcm (Nr. 63) | ||||||||||||||||||
| Gitterparameter |
a = 4,35 Å, b = 11,99 Å und c = 4,516 Å | ||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Caesiumhydroxid | ||||||||||||||||||
| Verhältnisformel | CsOH | ||||||||||||||||||
| Kurzbeschreibung |
weiße bis gelbe hygroskopische Kristalle[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 149,92 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
sehr leicht in Wasser (3000 g·l−1 bei 30 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 2 mg·m−3 (gemessen als einatembarer Staub)[3] | ||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Gewinnung und Darstellung
Caesiumhydroxid entsteht neben Wasserstoff bei der äußerst heftigen Reaktion (Explosionsgefahr) von Wasser mit Caesium:
Eine weitere Synthesemöglichkeit ist durch die Reaktion von Caesiumoxid mit Wasser gegeben.
Während der Vermischung können heftige Reaktionen auftreten.
Analog zum Rubidiumhydroxid ist auch das Caesiumhydroxid über das Sulfat zugänglich:
Das entstehende Bariumsulfat fällt quantitativ aus und die Caesiumhydroxidlösung kann nach der Filtration vorsichtig zunächst über Kaliumhydroxid in einer Platin-Schale eingeengt werden, bis sich das Salz abscheidet. Dieses wird schließlich in einem Silber-Schiffchen im trockenen Wasserstoff-Strom langsam auf 300 °C erhitzt.[4]
Eigenschaften
Wässrige Lösungen von Caesiumhydroxid reagieren stark basisch und ätzen Glas. Caesiumhydroxid kristallisiert orthorhombisch, Raumgruppe Cmcm (Raumgruppen-Nr. 63), mit den Gitterparametern a = 4,35 Å, b = 11,99 Å und c = 4,516 Å.[5] In der Kristallstruktur wird jedes Caesium-Kation von fünf Hydroxid-Anionen koordiniert, die Anionen koordinieren ihrerseits fünf Caesium-Ionen, so dass sich eine Schichtstruktur ergibt. Es sind auch Hydrate des Caesiumhydroxids bekannt. Das Monohydrat kristallisiert tetragonal, Raumgruppe I41/amd (Nr. 141)[6]. Es sind auch hexagonale Formen des Monohydrats beobachtet worden. Das Dihydrat, Cs(OH)·2 H2O kristallisiert orthorhombisch, Raumgruppe Pca21 (Nr. 29).[7] Das Trihydrat ist monoklin mit der Raumgruppe P21/n (Nr. 14, Stellung 2).[7]
Verwendung
Die Caesiumlauge ist eine hochwertige Base zur katalytischen Alkinylierung von Aldehyden und Ketonen.
Caesiumhydroxid wird als Elektrolyt in galvanischen Zellen verwendet.[8]



![{\displaystyle {2\,\mathrm {Cs} {}+{}2\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}2\,\mathrm {CsOH} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\uparrow {}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/f8e0b739bd1febd550a0ed46eabbf5965610bb9c)
![{\displaystyle {\mathrm {Cs} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}2\,\mathrm {CsOH} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/a094ddc7167a3501d887d7ef8f29c670056ad8d8)
![{\displaystyle {\mathrm {Cs} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {SO} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}\mathrm {Ba} (\mathrm {OH} ){\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {CsOH} {}+{}\mathrm {BaSO} {\vphantom {A}}_{\smash[{t}]{4}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/e4a6e283b4c8ac2547171dcc0a61a3fa39b72f31)