Diethyldicarbonat
chemische Verbindung
From Wikipedia, the free encyclopedia
Diethyldicarbonat, auch Diethylpyrocarbonat (DEPC), ist ein Ester der Pyrokohlensäure (Pyrocarbonat, Dicarbonat).
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
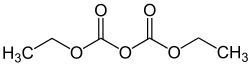 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Diethyldicarbonat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H10O5 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit fruchtigem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 162,14 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
1,12 g·cm−3 bei 25 °C[2] | |||||||||||||||
| Siedepunkt | ||||||||||||||||
| Löslichkeit |
langsame Zersetzung in Wasser[1] | |||||||||||||||
| Brechungsindex |
1,3960 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Verwendung
Diethyldicarbonat wird in der Biochemie und Molekularbiologie zur Inaktivierung von Ribonukleasen (RNasen) verwendet.[5] Bei der Herstellung RNase-freien Wassers wird diesem 0,1 % Diethyldicarbonat zugesetzt. Nach der Inkubation bei Raumtemperatur wird es anschließend autoklaviert. Unverbrauchtes Diethyldicarbonat hydrolysiert bei der Autoklavierung zu Ethanol und Kohlenstoffdioxid. Alternativ können manche fertigen Lösungen mit 0,05 % Diethyldicarbonat angesetzt werden und im Anschluss an eine 12 h Inkubation bei Raumtemperatur autoklaviert werden, wodurch auch mögliche RNase-Kontaminationen aus den Reagenzien inaktiviert werden, nicht aber in Anwesenheit von TRIS oder Thiolen.[6] RNase-freies Wasser wird bei der RNA-Reinigung und bei nachfolgenden Experimenten mit RNA verwendet.
Bis 1973 wurde Diethyldicarbonat in der Getränkeindustrie zur Kaltpasteurisation von Fruchtsäften, Wein und Bier verwendet (Kaltentkeimung). Diethyldicarbonat kann in wässrig-saurer Lösung und in Anwesenheit von Ammoniumionen (NH4+) Ethylurethan bilden, das von der IARC in die Kategorie 2A („wahrscheinlich krebserzeugend für den Menschen“) eingestuft ist.[7] Aus diesem Grund wurde 1973 der Zusatz von Diethyldicarbonat in Getränken verboten. Als Folgewirkstoff wird Dimethyldicarbonat eingesetzt.[8]
