Eu(tfc)3
chemische Verbindung
From Wikipedia, the free encyclopedia
Eu(tfc)3 (ehemals Eu(facam)3) ist eine enantiomerenreine organische Verbindung des Europiums, welches als gelb-oranges Pulver erscheint.[1]

| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
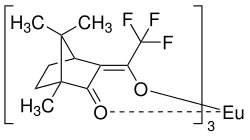 | |||||||||||||||||||
| Strukturformel des (+)-Enantiomers des Eu(tfc)3 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Eu(tfc)3 | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C36H42EuF9O6 | ||||||||||||||||||
| Kurzbeschreibung |
gelb-oranges Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 893,66 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Verwendung
Eu(tfc)3 wird vor allem in der NMR-Spektroskopie eingesetzt. Da es selbst enantiomerenrein ist, kann es diastereomere Aggregate mit anderen Stoffen bilden. So können im NMR, indirekt über das Diastereomerenverhältnis, Enantiomerenverhältnisse aufgeklärt werden. Außerdem kann es zur Bestimmung der absoluten Konfiguration von Alkoholen benutzt werden.[2]
Struktur und Eigenschaften
Es existieren beide Enantiomere des Eu(tfc)3, die sich entsprechend vom (+)- oder (−)-Campher ableiten. Viele Studien untersuchen jedoch nur das (+)-Enantiomer.[3][2] Die Gründe für die Verwendung von (+)-Campher sind vielfältig. So zeichnet sich die enantiomerenrein vorkommende Verbindung durch hohe Verfügbarkeit, Kristallinität und eine Vielzahl an möglichen Transformationen aus, die es erlauben, chirale Liganden herzustellen.[4]
Eu(tfc)3 ist strukturell eng mit Eu(hfc)3 verwandt und unterscheidet sich nur in der Länge des perfluorierten Rests am Campher-Grundgerüst. Die kürzere Kette im tfc-Liganden führt zu einer schlechteren Aufspaltung der Signale in NMR-Spektren.[3] Es ist löslich in Chloroform, aber unlöslich in Wasser.[5] Wie die meisten Lanthanoid-Shift-Reagenzien ist die Verbindung hygroskopisch.
Sicherheitshinweise
Starke Oxidationsmittel können starke Reaktionen mit Eu(tfc)3 hervorrufen. Fluorwasserstoff, Kohlenstoffmonoxid sowie Kohlenstoffdioxid und Europiumoxide sind die Zersetzungsprodukte der Verbindung.[1]
