LL-37
Protein
From Wikipedia, the free encyclopedia
LL-37 ist ein menschliches antimikrobielles Peptid aus der Gruppe der Cathelicidine. Es wird hauptsächlich in Immunzellen produziert und ist Teil der angeborenen Immunantwort sowie der Apoptose körpereigener Zellen. Es handelt sich um ein Transportprotein, dessen Einbau einerseits in die Zellwand grampositiver Bakterien sowie andererseits in die Zellmembran zu einem Verlust von Ionen und kleinen Molekülen führt. Es wird durch das CAMP-Gen codiert.[2]

| LL-37 | ||
|---|---|---|
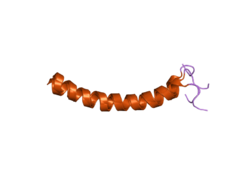 | ||
| 3D-Strukturmodell von LL-37 | ||
| Andere Namen |
| |
|
Vorhandene Strukturdaten: 2K6O | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 37 Aminosäuren | |
| Präkursor | (170 Aminosäuren) | |
| Bezeichner | ||
| Gen-Name | CAMP | |
| Externe IDs | ||
| Transporter-Klassifikation | ||
| TCDB | 1.C.33.1.10 | |
| Bezeichnung | Cathelicidin-Familie (Porine) | |
| Vorkommen | ||
| Übergeordnetes Taxon | Wirbeltiere[1] | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 820 | 12796 |
| Ensembl | ENSG00000164047 | ENSMUSG00000038357 |
| UniProt | P49913 | P51437 |
| Refseq (mRNA) | NM_004345 | NM_009921 |
| Refseq (Protein) | NP_004336 | NP_034051 |
| Genlocus | Chr 3: 48.22 – 48.23 Mb | Chr 9: 109.85 – 109.85 Mb |
| PubMed-Suche | 820 | 12796
|
Die Produktion von LL-37 wird insbesondere durch Stimulation des TLR-9, aber auch TLR-2 und TLR-4 und indirekt durch Vitamin D angeregt.[3][4]
Biosynthese
Die Biosynthese von LL-37 ist ein mehrstufiger Prozess. Es wird durch das CAMP-Gen auf Chromosom 3 codiert. Dieses Gen besteht, wie auch die Cathelicidin-Gene anderer Säugetiere, aus vier Exons. Die antimikrobielle Aktivität wird durch das hypervariable Exon 4 codiert, während die Exons 1 bis 3 eine Signalpeptidsequenz und die darauf folgende Cathelin-Domäne codieren.[5]
Primär wird ein Präpropeptide synthetisiert und in den Granula neutrophiler Granulozyten oder anderer Zellen gespeichert. Nach Freisetzung dieser biologisch inaktiven Propeptide werden sie enzymatisch durch Elastase oder andere Proteinasen in ein Cathelin und ein C-terminales antimikrobielles Peptid, das aus 37 Aminosäuren bestehende LL-37, gespalten.
Im Einbuchstabencode lautet die Peptidsequenz von LL-37 LLGDFFRKSKEKIGKEFKRIVQRIKDFLRNLVPRTES.[6]
Literatur
Zanetti M: The role of cathelicidins in the innate host defenses of mammals. In: Curr Issues Mol Biol. 7. Jahrgang, Nr. 2, Juli 2005, S. 179–96, PMID 16053249 (horizonpress.com [PDF]).