Lithiumamid
chemische Verbindung
From Wikipedia, the free encyclopedia
Lithiumamid ist eine chemische Verbindung des Lithiums aus der Stoffgruppe der Metallamide.

| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
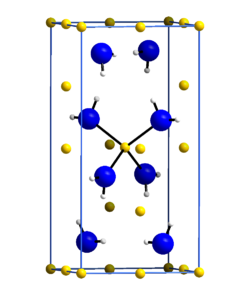 | ||||||||||||||||
| _ Li+ _ N3− _ H+ | ||||||||||||||||
| Kristallsystem | ||||||||||||||||
| Raumgruppe |
I4 (Nr. 82) | |||||||||||||||
| Gitterparameter | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Lithiumamid | |||||||||||||||
| Verhältnisformel | LiNH2 | |||||||||||||||
| Kurzbeschreibung |
farb- und geruchloser Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 22,96 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
1,178 g·cm−3 (20 °C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
430 °C[2] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Gewinnung und Darstellung
Lithiumamid wird industriell durch Erhitzen von Lithium oder Lithiumhydrid in einem Strom von Ammoniak hergestellt. Außerdem bildet es sich langsam, wenn Lithium in flüssigem Ammoniak gelöst wird.[5] Wie auch bei anderen Alkali- und Erdalkaliamiden wird diese Reaktion durch die Anwesenheit von Eisen(II)-chlorid erheblich beschleunigt.[6]
Eigenschaften
Lithiumamid ist ein farb- und geruchloser Feststoff, der sich in Wasser zersetzt.[2]
Die Verbindung ist allgemein sehr hydrolyseempfindlich und greift Glas schwach an.[3][7] Beim Erhitzen im Vakuum gibt sie oberhalb von 300 °C Ammoniak ab. Der quantitative Abbau zu Lithiumimid erfolgt jedoch erst bei 400 °C und erst oberhalb 750–800 °C zersetzt sie sich unter Abgabe von Stickstoff, Wasserstoff und Ammoniak.[7]
Kristallstruktur
Die Kristallstruktur des Lithiumamids wurde im Jahr 1951 von Robert Juza und Karl Opp in der tetragonalen Raumgruppe I4 (Nr. 82) mit a = 501,6 pm und c = 1022 pm anhand von Pulveraufnahmen bestimmt[8]. Hierbei wurde die Lage der Stickstoffatome und der Lithiumatome bestimmt, jedoch nicht des Wasserstoffs. In einer späteren Arbeit im Jahre 1972 wurde die Kristallstruktur anhand eines Lithiumamid-Einkristalls neu bestimmt. Hierbei wurden auch die Lagen der Wasserstoffatome bestimmt. Die Gitterparameter wurden zu a = 503,7 pm und c = 1027,8 pm bestimmt. Die Stickstoffatome bilden eine verzerrte kubisch dichteste Kugelpackung, in der jede zweite Tetraederlücke von Lithium besetzt ist. Die ABC-Abfolge der Schichten ist entlang [112] angeordnet. In z = 0 sind es drei Li+, in z = 1/4 ein Li+, in z = 1/2 wieder drei Li+ und in z = 3/4 wieder ein Li+. Die Struktur steht in Verwandtschaft zu der des Lithiumhydroxides, unterscheidet sich aber von dieser.[9][10]
Verwendung
Lithiumamid wird in der organischen Chemie bei Claisen-Kondensationen, bei der Alkylierung von Nitrilen und Ketonen sowie der Synthese von Ethinyl-Verbindungen und Carbinolen verwendet.[5] Sie wird weiterhin als Reagenz zur Kreuzkupplung von Arylchloriden und Aminen eingesetzt.[11]





