Methoxychlor
chemische Verbindung
From Wikipedia, the free encyclopedia
Methoxychlor ist eine Mischung mehrerer strukturisomerer chemischer Verbindungen aus der Gruppe der chlorierten Diphenylmethanderivate. Es ist u. a. das p,p′-Dimethoxy-Analogon von p,p′-DDT.

| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
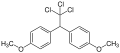
| Strukturformel von p,p′-Methoxychlor | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Methoxychlor | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C16H15Cl3O2 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser bis gelblicher Feststoff mit fruchtigem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 345,66 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,41 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
etwa 346 °C[2] | ||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (0,1 mg·l−1 bei 25 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 10 mg·m−3 (gemessen als einatembarer Staub)[3] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Gewinnung und Darstellung
Methoxychlor kann durch Reaktion von Anisol mit Chloral in Gegenwart von Aluminiumchlorid oder Schwefelsäure gewonnen werden.[4]
Eigenschaften
Methoxychlor ist ein brennbarer farbloser bis gelblicher Feststoff mit fruchtigem Geruch, der praktisch unlöslich in Wasser ist.[1] In Reinform ist es ein farbloses Pulver. Das technische Produkt ist grau bis gelblich und besteht zu 88–90 % aus dem p,p′-Isomer. Der Rest besteht hauptsächlich aus dem o,p′-Isomer und bis zu 50 anderen Verunreinigungen.[5]
- p,p′-Methoxychlor, 88–90 % des technischen Gemischs
- o,p′-Methoxychlor, 4 % des technischen Gemischs
- 1-Methoxy-4-(1,2,2,2-tetrachlorethyl)benzol, 1,7 % des technischen Gemischs
- p,p′-Methoxychlor-olefin, 0,4 % des technischen Gemischs
Die Verbindung wurde zuerst 1944 beschrieben und 1945 eingeführt.[6]
Toxizität
In einigen In-vivo-Studien scheint „technisches“ Methoxychlor drei- bis viermal wirksamer bezüglich der Reproduktions- und Entwicklungstoxizität zu sein als reines Methoxychlor. Dies wird darauf zurückgeführt, dass Verunreinigungen im „technischen“ Methoxychlor, welche teilweise Metaboliten[7] von Methoxychlor sind, direkt östrogen wirksame Substanzen sind. Methoxychlor selbst wirkt schwach östrogen.[8]

Dabei stellte sich vor allem der durch das Cytochrom P450 in der Leber demethylierte Metabolit von Methoxychlor 2,2-Bis(p-hydroxyphenyl)-1,1,1-trichlorethan (HPTE oder Hydroxychlor) als ein potenter endokriner Disruptor heraus.[9] Neuere Studien bei Ratten zeigen, dass Methoxychlor Krankheiten noch bis in die dritte Folgegeneration auslösen kann.[10][11]
Verwendung
Methoxychlor wurde als Insektizid verwendet.[1]
Zulassung
Die Verbindung wurde 2002 nicht in die Liste der in der Europäischen Union zulässigen Pflanzenschutzwirkstoffe aufgenommen. In den Staaten der EU und in der Schweiz sind keine Pflanzenschutzmittel mit diesem Wirkstoff zugelassen.[12] Das Europäische Arzneibuch legt als Grenzwert für Methoxychlor-Rückstände in pflanzlichen Drogen 0,05 mg·kg−1 fest.[13]
Die Genehmigung zur Verwendung als Pflanzenschutzmittel oder Biozid in den USA wurde 2003 entzogen.[14] Grund für das Verbot war seine Persistenz in der Umwelt und des Akkumulationsvermögen in der Nahrungskette. 2023 wurde Methoxychlor in den Anhang A des Stockholmer Übereinkommens aufgenommen.[15]