Pinnick-Oxidation
From Wikipedia, the free encyclopedia
Die Pinnick-Oxidation ist eine chemische Reaktion durch welche Aldehyde in die entsprechenden Carbonsäuren oxidiert werden können. Sie verläuft unter Nutzung von Natriumchlorit und unter mild sauren Bedingungen. Die Reaktion wurde ursprünglich von Bengt O. Lindgren und Nilsson entwickelt.[1] Die heutzutage typischen Reaktionsbedingungen sind die von G. A. Kraus.[2][3] H. W. Pinnick zeigte später, dass diese Bedingungen auf die Oxidation α,β-ungesättiger Aldehyde angewendet werden können.[4] Es existieren viele verschiedene Reaktionen um Aldehyde zu oxidieren, aber nur wenige sind bei einer breiten Menge an funktionellen Gruppen anwendbar. Die Pinnick-Oxidation hat sich sowohl als Methode mit hoher Funktionelle-Gruppen-Toleranz erwiesen als auch für Reaktionen an sterisch gehinderten Gruppen. Ein weiterer Vorteil sind die geringen Kosten.[4][5]
Mechanismus
Der postulierte Reaktionsmechanismus geht von chloriger Säure als aktives Oxidans aus, welche sich unter sauren Bedingungen aus dem Chlorit bildet.
- ClO2− + H2PO4− → HClO2 + HPO42−
Als erstes addiert die Chlorige Säure an den Aldehyd. Die resultierende Struktur geht eine pericyclische Fragmentierung ein, in welcher das Aldehyd-Wasserstoffatom auf ein Sauerstoffatom des Chlorits übertragen wird. Dabei eliminiert Hypochlorige Säure.[6]
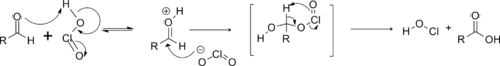
Nebenreaktionen und Scavenger
Das Nebenprodukt HOCl, immer noch ein reaktives Oxidationsmittel, kann auf verschiedene Arten problematisch sein.[6] Es kann mit dem Reagenz NaClO2 abreagieren und Chlordioxidgas bilden, wodurch das NaClO2 nicht mehr für das fortschreiten der gewünschten Oxidationsreaktion herhalten kann:
- HOCl + 2ClO2− → 2ClO2 + Cl− + OH−
Auch mit den organischen Komponenten der Reaktionsmischung können weitere Nebenreaktionen ablaufen. Zum Beispiel addiert HOCl an Doppelbindungen unter Bildung von Halohydrinen.
Um die von HOCl ausgehenden Nebenreaktionen zu verhindern wird üblicherweise ein Scavenger eingesetzt, der bevorzugt mit HOCl reagiert und es so aus dem Gleichgewicht entfernt. Zum Beispiel kann man hierzu von der Präferenz des HOCl, an Doppelbindungen zu addieren, Gebrauch machen, indem ein „Opfer-Alken“ der Reaktionsmischung beigefügt wird. 2-Methyl-2-buten ist hierbei das Reagenz der Wahl.

Resorcin und Sulfamsäure sind ebenfalls gebräuchliche Scavenger.[6][7]
Wasserstoffperoxid ist in der Pinnick-Oxidation ein Scavenger, dessen Nebenprodukte die Hauptreaktion nicht stören:
- HOCl + H2O2 → HCl + O2 + H2O
Unter schwach sauren Bedingungen geht konzentriertes H2O2 (35 %) eine schnelle Oxidationsreaktion ohne kompetitive Reduktion von HClO2 zu HOCl.
- HClO2 + H2O2 → HOCl + O2 + H2O
Chlordioxid reagiert schnell mit H2O2 und bildet Chlorige Säure.
- 2ClO2 + H2O2 → 2HClO2 + O2
Die Bildung von Sauerstoff ist somit auch ein guter Indikator für das Fortschreiten der Reaktion. Dennoch kommt es manchmal zu Problemen durch Bildung von Singulett-Sauerstoff, welcher generell organische Stoffe oxidiert (siehe Schenck-En-Reaktion). In Fällen, bei denen H2O2 nicht zu hohen Ausbeuten führte, wurde stattdessen oft DMSO verwendet. Elektronenreiche Aldehyde fallen hauptsächlich unter diese Kategorie.[7]
Es wurden auch schon Versuche mit Festphasen-Reagenzien wie z. B. Phosphat-gepuffertem Silicagel mit Kaliumpermanganat und Polymer-gebundenes Chlorit durchgeführt um Aldehyde zu Carbonsäuren zu überführen ohne die herkömmliche Aufarbeitungsprozedur durchführen zu müssen. Solche Reaktionen verlaufen allerdings unter Bindung des Produkts an das Silicagel in Form ihres Kaliumsalzes. Neutrale Verunreinigungen können daher mit organischen Lösungsmitteln weggewaschen werden.[8]
Anwendungsbereich und Einschränkungen
Die Reaktion ist für Substrate mit vielen verschiedenen funktionellen Gruppen geeignet. β-Arylsubstituierte α,β-ungesättigte Aldehyde lassen sich unter den Reaktionsbedingungen gut umsetzen. Auch Substrate mit Dreifachbindungen, welche direkt mit dem Aldehyd oder anderen Doppelbindungen konjugiert sind können eingesetzt werden.[7][9] Alkohole, Epoxide, Benzylether und Halogenorganische Verbindungen, sogar Stannane sind gegen die Reaktionsbedingungen stabil.[7][9][10][11] Die unten gezeigten Beispiele zeigen, dass sowohl die Konfiguration der Stereozentren der α-Kohlenstoffatome als auch der Doppelbindungen (vor allem dreifachsubstituierter) unverändert bleiben.

Niedrigere Ausbeuten werden bei Reaktionen an aliphatischen α,β-ungesättigten oder hydrophilen Aldehyden erhalten. Substrate mit Doppelbindungen oder elektronenreichen Aldehyden können Chlorierung als Nebenreaktion hervorrufen. In solchen Fällen erhält man mit DMSO als Scavenger bessere Ausbeuten. Ungeschützte aromatische Amine und Pyrrole sind ebenfalls schlecht geeignete Substrate. Besonders α-Aminoaldehyde reagieren schlecht wegen Epimerisierung und weil Aminogruppen leicht zu den entsprechenden N-Oxiden umgesetzt werden. Typische Schutzgruppenchemie wie z. B. die Verwendung von Boc kann für solche Probleme eine Lösung sein.[12]
Thioether sind hochreaktiv in der Pinnick-Oxidation. Zum Beispiel führt die Reaktion von Thioanisaldehyd zu hohen Ausbeuten von Carbonsäureprodukten, allerdings unter gleichzeitigem Umsatz des Thioethers zum Sulfoxid oder Sulfon.[7]

