Plumbylene
Divalente Bleiverbindungen
From Wikipedia, the free encyclopedia
Plumbylene (oder Plumbylidene) sind divalente Blei(II)organyle und Tetrylene mit der generellen chemischen Formel R2Pb. Plumbylene haben sechs Elektronen in ihrer Valenzschale und sind niedervalente Verbindungen.

Das erste beschriebene Plumbylen war das Dialkylplumbylen [(Me3Si)2CH]2Pb, welches 1973 von Michael Lappert und Mitarbeitern synthetisiert wurde.[1]
Plumbylene können als kohlenstoffsubstituierte Plumbylene, Plumbylene, die durch ein Gruppe 15 oder 16 Element stabilisiert werden, und als monohalogenierte Plubylene klassifiziert werden.[2]
Synthese
Plumbylene können zum einen durch Transmetallierung von Bleidihalogeniden mit lithiumorganischen Verbindungen oder Grignardreagenzien synthetisiert werden.[2] Das erste Plumbylen [((CH3)3Si)2CH]2Pb von Michael Lappert et al. wurde entsprechend durch die Reaktion von Bleidichlorid mit [((CH3)3Si)2CH]Li erhalten.[1] Die äquimolare Zugabe von Lithiumorganylen zu Bleidihalogeniden führt zu monohalogenierten Plumbylenen, die Zugabe von zwei Äquivalenten Lithiumorganylen zu diorganylsubstituierten Plumbylenen.[3] Auf diese Weise können Dialkyl-,[1] Diaryl-,[4] Diamido-,[5] Dithioplumbylene[3] erhalten werden. Die Zugabe einer Organolithium- oder Grignard-Verbindung mit einem unterschiedlichen organischen Substituenten zu monohalogenierten Plumbylenen führt zum Erhalt von heteroleptischen Plumbylenen.[3]

Auch die Transmetallierung von [((CH3)3Si)2N]2Pb kann zur Synthese von Diarylplumbylenen,[6] Disilylplumbylenen,[7] und gesättigten N-heterocyclischen Plumbylenen[8] verwendet werden.

Alternativ können Plumbylene auch durch die reduktive Dehalogenierung von tetravalenten Organobleiverbindungen (R2PbX2).[6]

Struktur und Bindung

Ein Kernaspekt der elektronischen Struktur von Plumbylenen und damit ihrer Reaktivität hängt mit dem Inert-Pair-Effekt zusammen. So führt der wachsende Abstand zwischen den Energien der s- und p-Orbitale bei zunehmender Ordnungszahl der Elemente der Gruppe 14 zusammen mit einer starken relativistischen Kontraktion des 6s-Orbitals nur zu einem geringen Hybridisierungsgrad der s- und p-Orbitale. In der Folge liegt das 6s-Orbital energetisch sehr niedrig und ist verhältnismäßig inert.[9] Das führt in der Konsequenz dazu, dass Plumbylene einen Singulettzustand einnehmen, eine hohe Energiedifferenz zwischen Singulett- und Triplett-Zustand aufweisen und in Lösung zu einem Gleichgewicht zwischen monomerer und dimerer Form neigen (siehe unten).[9] Das steht im Gegensatz zu Carbenen, die häufig einen Triplettgrundzustand aufweisen und leicht zu Alkenen dimerisieren.

In Dimethylblei (CH3)2Pb beträgt die the Pb–C-Bindungslänge 2.267 Å und der C–Pb–C-Bindungswinkel 93.02°. Der Singulett-Triplett-Abstand beträgt 36,99 kcal mol−1.[10]
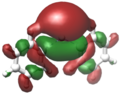
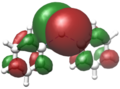
Verschiedene Visualisierungsmethoden wie Kohn-Sham-Orbitale oder NBOs zeigen bei Diphenylblei Ph2Pb eine deutliche Lokalisation eines freien Elektronenpaares in Form des höchsten besetzten Molekülorbitals (HOMO) am Bleizentrum. Ebenso findet sich dort das niedrigste unbesetzte Molekülorbital (LUMO).[11]
- HOMO von Ph2Pb
- LUMO von Ph2Pb
- Das mittels NBO berechnete freie 6s-Elektronenpaar
- Das mittels NBO berechnete vakante 6p-Orbital
Die Pb–C-Bindungslängen betragen in dieser Verbindung 2.303 Å und der C–Pb–C-Bindungswinkel 105.7°. Ungeachtet von verschiedenen theoretischen Rechenniveaus kann der größere Bindungswinkel in Diphenylblei gegenüber Dimethylblei auf die Abstoßung der sterisch anspruchsvolleren Phenylgruppen zurückgeführt werden.
Plumbylene treten als reaktive Intermediate bei der Bildung von tetravalenten Plumbanen (R4Pb) auf.[12] Obwohl der Inert-Pair-Effekt darauf deutet, dass die divalenten Spezies thermodynamisch stabiler sein sollten, kann die Abwesenheit von stabilisierenden Substituenten zu einer Sensitivität gegenüber Licht und Wärme und damit zu Polymerisation und Disproportionierung führen. Entsprechend entsteht bei einer solchen Reaktion auch elementares Blei.[12][13]
Plumbylene können als Monomere durch die Verwendung von sterisch anspruchsvollen Liganden (kinetische Stabilisierung) oder hetreroatomhaltigen Substituenten, die Elektronendichte in das vakante 6p-Orbital donieren (thermodynamische Stabilisierung), stabilisiert werden.[2]
Elektronische Stabilisierung von Plumbylenen
Plumbylene können durch funktionelle Gruppen stabilisiert werden, die Elektronendichte in das vakante 6p-Orbital des Bleis donieren. Die geläufigsten intramolekularen Wege sind zum einen die Einführung einer funktionellen Gruppe mit einem dem Blei benachbarten Atom, das ein freies Elektronenpaar besitzt, oder die Koordination einer Lewis-basischen Funktionalität aus einer anderen Stelle des Moleküls.[14]
Ein Beispiel für den ersten Fall sind dem Blei benachbarte Elemente der Gruppen 15 und 16, analog zu Fischer-Carbenen oder N-heterocyclischen Carbenen.[2][4][15][16]

Beispiele für den zweiten Fall sind zum Beispiel koordinierende Aminogruppen aus dem Rückgrat des Moleküls.[14] Allerdings gibt es sogar Beispiele für die Koordination von Fluoratomen aus Trifluormethylgruppen.[17]
- Stabilisierung eines Plumbylens durch die Koordination einer Amingruppe eines Substituenten
- Lewisstruktur von [2,4,6-(CF3)3C6H2]2Pb
- Molekülstruktur von [2,4,6-(CF3)3C6H2]2Pb im Kristall
Agostische Wechselwirkungen
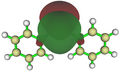
Auch agostische Wechselwirkungen können Plumbylene stabilisieren. So zeigten computerchemische Untersuchungen von {[R(Me3)2Si][Me2P(BH3)]CH}2Pb (R = Me oder Ph), dass die Wechselwirkungen von bindenden B–H-Orbitalen mit dem vakanten 6p-Orbital die Energie des Moleküls um etwa 38 kcal mol−1 senken. Diese Beobachtung wurde durch Kristallstrukturanalysen untermauert, in denen die B–H Bindungen nur einen geringen Abstand zum Blei aufweisen.[18]
- Frontansicht von {(Me3Si)[Me2P(BH3)]CH}2Pb
- Draufsicht auf {(Me3Si)[Me2P(BH3)]CH}2Pb
Reaktivität
Wie oben erwähnt tendieren unstabilisierte Plumbylene zu Polymerisation, Disproportionierung oder Dimerisierung. Allerdings gibt es noch eine Vielzahl weiterer Reaktivitäten.
Bildung von Lewis-Säure-Base-Addukten
So verhalten sich Plumbylene durch das vakante 6p-Orbital Lewis-sauer und neigen entsprechend dazu, Addukte mit Lewisbasen wie Trimethylaminoxid,[19] 1-Azidoadamantan (AdN3)[20] oder Mesitylazid (MesN3)[19] zu bilden. Im Gegensatz dazu führt die Reaktion von Stannylenen und Trimethylaminoxid durch eine Oxidation des Zinns von der Oxidationsstufe +II auf +IV zum korrespondierenden Zinnoxid. Das lässt sich auf den deutlich schwächeren Inert-Pair-Effekt des Zinns und einer damit verbundenen Vorliebe zur Oxidation zurückführen.[21]
Dimerisierung

Plumbylene können auf zwei Wegen dimersieren. Zum einen durch die Bildung von Pb=Pb-Doppelbindungen und damit der Bildung von Diplumbylenen, zum anderen aber auch verbrückt durch Halogen–Blei-Wechselwirkungen. Nichthalogenierte Plumbylene liegen in Lösung in einem Gleichgewicht zwischen monomerer und dimerer Form vor. Im Festkörper können sie aufgrund von geringen Dimerisierungsenergien sowohl als monomere oder als dimere Vorliegen. Das ist in der Regel vom sterischen Anspruch der Substituenten abhängig.[2][9][22][23] Allerdings große Substituenten auch zu einer sterischen Verhinderung der Dimerisierung und damit zum reinen Vorliegen des Monomers führen.[3][23][24]

Die Triebkraft der Dimerisierung lässt sich auf die amphotere Lewisverhalten von Plumbylenen zurückführen. So kann das freie 6s-Elektronenpaar als Lewisbase und Elektronendonor dienen, wohingegen das vakante 6p-Orbital als Lewissäure und Elektronenakzeptor fungieren kann.[7][11] Diplumbylene weisen in der Folge eine trans-bent-Struktur, ähnlich zu den leichteren Homologen (Disilylene, Digermylene, Distannylene) auf.[9] Dabei sind die beobachteten Pb–Pb-Bindungen (2,90–3,53 Å) tendenziell länger als in Diblumbanen R3PbPbR3 (2,84–2,97 Å).[23] Dieses kontraintuitive Verhalten lässt sich auf zwei 6s-6p-Donor-Akzeptor-Wechselwirkungen zurückführen, die energetisch günstiger sind als der Überlapp von spn-Orbitalen mit einem höheren Hybridisierungsgrad.[23]
In monohalogenierten Plumbylenen ist außerdem das Halogenatom dazu in der Lage Elektronendichte in das vakante 6p-Orbital an einem Bleiatom eines zweiten Plumbylens zu donieren, wodurch verbrückte Spezies entstehen. Solche monohalogenierten Plumbylene liegen im Allgemeinen in Lösung monomer und im Festkörper als Dimer vor, allerdings kann auch hier ein hoher sterischer Anspruch der Substituenten die Dimerisierung verhindern.[2] Da die Dimerisierungsenergie von Tetrylenen in der Gruppe 14 mit steigender Ordnungszahl des Zentralatoms abnimmt, dimerisieren monohalogenierte Stannylene und Plumbylene eher verbrückend als monohalogenierte Silylene und Plumbylene. Letztere dimersieren eher über die oben beschriebenen Doppelbindungen.[2]

Insertionsreaktionen
Ähnlich zu Carbenen[25] und den anderen Tetrylenen[2] können Plumbylene Insertionsreaktionen eingehen. Insbesondere sind Insertionen in C–X- (X = Br, I) und E–E-Bindungen der Gruppe 16 (E = S, Se) bekannt.[6]

Transmetallierung
Plumbylene können weiterhin nukleophile Substitutionsreaktionen mit metallorganischen Reagenzien eingehen. So begehen sie zum Beispiel mit geeigneten Gruppe 13-Verbindungen entsprechende Metathesen.[24]

Plumbylene mit unterschiedlichen Substituenten können ebenso Transmetallierungsreaktionen eingehen und ihre Substituenten austauschen. Die Triebkraft dieser Reaktion ist die geringere sterische Spannung im Produkt bei einer gleichzeitig geringen Dissoziationsenergie der Pb–C-Bindung.[26]

Anwendung

Plumbylene können außerdem als σ-Donor-σ-Akzeptorliganden in Metallkomplexen eingesetzt werden. Die σ-Donorfuktionalität resultiert dabei aus dem besetzten 6s-Orbital und die σ-Akzeptorfunktionalität aus dem unbesetzten 6p-Orbital.
Bei Raumtemperatur stabile Plumbylene können außerdem als Precursoren in der chemischen Gasphasenabscheidung oder der Atomlagenabscheidung eingesetzt werden, um bleihaltige Materialien zu erhalten.[27] Dithioplumbylene und Dialkoxyplumbylene könnten außerdem sinnvolle Ausgangsmaterialien für den Halbleiter Blei(II)-sulfid beziehungsweise das piezokeramische Blei-Zirkonat-Titanat sein.[28]



![Lewisstruktur von [2,4,6-(CF3)3C6H2]2Pb](http://upload.wikimedia.org/wikipedia/commons/thumb/2/2c/%282%2C4%2C6-%28CF3%293C6H2%292Pb_skeletal.png/250px-%282%2C4%2C6-%28CF3%293C6H2%292Pb_skeletal.png)
![Molekülstruktur von [2,4,6-(CF3)3C6H2]2Pb im Kristall](http://upload.wikimedia.org/wikipedia/commons/thumb/d/dc/%282%2C4%2C6-%28CF3%293C6H2%292Pb_X-ray.png/250px-%282%2C4%2C6-%28CF3%293C6H2%292Pb_X-ray.png)
![Frontansicht von {(Me3Si)[Me2P(BH3)]CH}2Pb](http://upload.wikimedia.org/wikipedia/commons/thumb/7/70/Plumbylene_agostic_front_view2.png/250px-Plumbylene_agostic_front_view2.png)
![Draufsicht auf {(Me3Si)[Me2P(BH3)]CH}2Pb](http://upload.wikimedia.org/wikipedia/commons/thumb/f/f8/Plumbylene_agostic_top_view2.png/250px-Plumbylene_agostic_top_view2.png)