Rad51
Protein in Homo sapiens
From Wikipedia, the free encyclopedia
Rad51 ist ein DNA-bindendes Protein in Eukaryonten und ein Mitglied der RAD51-Protein-Familie, die eine Funktion in der DNA-Reparatur bei Doppelstrangbrüchen hat. RAD51-Proteine sind Homologe zu den bakteriellen Proteinen RecA und zum Rad51 aus der Bäckerhefe. Die Proteinsequenz ist sehr stark konserviert, d. h. die Aminosäuresequenzen der jeweiligen Proteine ähneln sich von Hefen bis Menschen. Im Allgemeinen findet sich bei Eukaryoten (komplex-zellulären Organismen) neben Rad51 auch DMC1 als homologes Protein, bei Archaeen dagegen RadA und im Bakteriophagen T4 schließlich UvsX .[1]

| Rad51 | ||
|---|---|---|
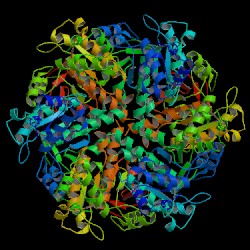 | ||
| Kristallstruktur eines Rad51-Filaments nach PDB 1SZP | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 26,4 - 37,0 Kilodalton / 280 - 340 Aminosäuren (je nach Isoform) | |
| Isoformen | 4 | |
| Bezeichner | ||
| Gen-Namen | RAD51, BRCC5, FANCR, HRAD51, HsRad51, HsT16930, MRMV2, RAD51A, RECA | |
| Externe IDs | ||
| Vorkommen | ||
| Homologie-Familie | Hovergen | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 5888 | 19361 |
| Ensembl | ENSG00000051180 | ENSMUSG00000027323 |
| UniProt | Q06609 | Q08297 |
| Refseq (mRNA) | NM_001164269 | NM_011234 |
| Refseq (Protein) | NP_001157741 | NP_035364 |
| Genlocus | Chr 15: 40.69 – 40.73 Mb | Chr 2: 119.11 – 119.15 Mb |
| PubMed-Suche | 5888 | 19361
|
Varianten
Es gibt zwei alternativ gespleißte Varianten des Gens, die jeweils für verschiedene Proteine kodieren. Transkriptionsvarianten, die alternative Poly-A-Signale verwenden, existieren ebenso.
Funktionen
Im Menschen ist RAD51 ein 339 Aminosäuren langes Protein, das eine Hauptrolle in der homologen Rekombination der DNA bei der Doppelstrangbruch-Reparatur spielt. Dabei wird unter ATP-Verbrauch ein DNA-Strang ausgetauscht, indem ein DNA-Strang in eine basengepaarte homologe DNA-Sequenz eingefügt wird. RAD51 sucht nach homologen Bereichen und hilft bei der DNA-Anlagerung.
Die Familie der RecA/Rad51-Proteine formt ein helicales Nukleoproteinfilament auf der DNA.[2] Die Struktur dieser Rad51-Filament-Formation der funktionelle Mechanismus ist noch nicht vollständig aufgeklärt. Studien, die fluoreszierendes RAD51 benutzten,[3] haben gezeigt, dass Rad51-Fragmente sich verlängern und wachsen, bis sie etwa 2 µm an Länge erreicht haben. Die Dissoziation des Rad51 von der dsDNA ist dagegen langsam und inkomplett, sodass ein anderer Mechanismus dabei mitwirken könnte.
Pathologie
Da das Protein mit PALB2[4] und BRCA2 interagiert, ist es möglicherweise wichtig für die Antwort der Zelle auf DNA-Schäden. BRCA2 reguliert die intrazelluläre Position und DNA-Bindefähigkeit des RAD51. Der Verlust dieser Kontrolle, gefolgt von BRCA2-Inaktivierung könnte ein Schlüsselereignis sein, das zu genomischer Instabilität und Tumorentstehung führen kann.[5]
Das Rad51-Gen befindet sich beim Menschen auf Chromosom 15 und einige Veränderungen wurden mit einem erhöhten Brustkrebsrisiko in Verbindung gebracht. Die an Brustkrebs vielleicht beteiligten Proteine BRCA2 und PALB2 kontrollieren die Funktion von Rad51 während der DNA-Reparatur durch homologe Rekombination.[4][6]
Erhöhte RAD51-Expression wurde in Mammakarzinomen von Hunden entdeckt, was darauf hindeutet, dass eine genomische Instabilität eine wichtige Rolle bei diesem Tumortyp spielt.[7][8][9][10]