Acetato de magnesio
From Wikipedia, the free encyclopedia
16674-78-5 (tetrahidrato)[1]
| Acetato de magnesio | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Etanoato de magnesio | ||
| General | ||
| Fórmula semidesarrollada | Mg(CH3COO)2 | |
| Fórmula estructural |
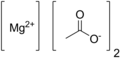 | |
| Fórmula molecular | Mg(C2H3O2)2 | |
| Identificadores | ||
| Número CAS |
142-72-3 (Anhídro) 16674-78-5 (tetrahidrato)[1] | |
| ChEBI | 62964 | |
| ChEMBL | 1200691 | |
| ChemSpider | 8556 | |
| DrugBank | DB13996 | |
| PubChem | 8896 | |
| UNII | 0E95JZY48K | |
| Propiedades físicas | ||
| Apariencia | cristales blancos higroscopicos | |
| Densidad | 1450 kg/m³; 1,45 g/cm³ | |
| Masa molar | 142,394 g/mol | |
| Punto de fusión | 80 °C (353 K) | |
| Propiedades químicas | ||
| Solubilidad en agua | soluble | |
| Compuestos relacionados | ||
| Otros Cationes | Acetato de calcio | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El acetato de magnesio anhidro tiene la fórmula química Mg(CH3COO)2 y, en su forma hidratada, acetato de magnesio tetrahidratado, su fórmula química es Mg(CH3COO)2·4H2O. En este compuesto, el magnesio tiene un estado de oxidación de +2. El acetato de magnesio es la sal de magnesio del ácido acético.[2] Este es delicuescente y, al calentarse, se descompone para formar óxido de magnesio.[3] El acetato de magnesio se utiliza comúnmente como fuente de magnesio en reacciones biológicas.[4]
El acetato de magnesio se presenta en forma de cristales higroscópicos blancos. Huele a ácido acético y es soluble en agua. En solución acuosa, su pH es alcalino, casi neutro.[5][6]
Almacenamiento
Debido a su alta higroscopicidad, debe almacenarse lejos del agua. Además, es incompatible con oxidantes fuertes y no debe mezclarse con ellos.[5]
Síntesis
Síntesis de acetato de magnesio a partir de la reacción de hidróxido de magnesio con ácido acético.[7]
- 2 CH
3COOH + Mg(OH)
2 → Mg(CH
3COO)
2 + 2 H
2O
también se puede prepararse, haciendo una suspensión de carbonato de magnesio en agua destilada con solución de ácido acético al 20%.[8]
- 2 CH
3COOH + MgCO
3 → Mg(CH
3COO)
2 + CO
2 + H
2O
La reacción usando magnesio metálico con ácido acético disuelto en benceno seco, provoca la formación de acetato de magnesio junto con la liberación de hidrógeno gaseoso.[9]
- Mg + 2CH
3COOH → Mg(CH
3COO)
2 + H
2