Acoplamiento de Negishi
El acoplamiento de Negishi es una reacción de acoplamiento cruzado catalizada por metales de transición ampliamente utilizada. La reacción acopla halocarburos o triflatos con compuestos organometálicos de zinc, formando enlaces carbono-carbono (C-C) en el proceso. Generalmente se utiliza una especie de paladio (0) como catalizador metálico, aunque a veces se usa níquel. Se puede emplear una variedad de catalizadores de níquel en estado de oxidación Ni0 o NiII en acoplamientos cruzados de Negishi como Ni(PPh3)4, Ni(acac)2, Ni(COD)2, etc.
-
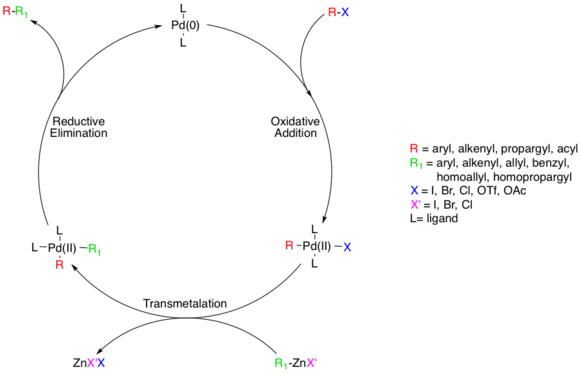
- El grupo saliente X suele ser cloruro, bromuro, o yoduro, pero también son factibles los grupos triflato and acetiloxi. Generalmente, si X = Cl conduce a reacciones lentas.
- El residuo orgánico R = alquenilo, arilo, alilo, alquinilo o propargilo.
- El haluro X' en el compuesto de organozinc puede ser cloruro, bromuro o yoduro y el residuo orgánico R' es alquenilo, arilo, alilo, alquilo, bencilo, homoalilo, and homopropargilo.
- El metal M en el catalizador es níquel o paladio.
- El ligando L en el catalizador puede ser trifenilfosfina, dppe, BINAP o chiraphos. Los catalizadores de paladio en general tienen mayores rendimientos químicos y mayor tolerancia a los grupos funcionales. El acoplamiento de Negishi encuentra un uso común en el campo de la síntesis total como un método para formar selectivamente enlaces C-C entre intermediarios sintéticos complejos. La reacción permite el acoplamiento de átomos de carbono sp, sp y sp (ver hibridación orbital), lo que la hace algo inusual entre las reacciones de acoplamiento catalizadas por paladio. Los organozincs son sensibles a la humedad y al aire, por lo que el acoplamiento de Negishi debe realizarse en un ambiente libre de oxígeno y agua, un hecho que ha dificultado su uso en relación con otras reacciones de acoplamiento cruzado que requieren condiciones menos robustas (como la reacción de Suzuki). Sin embargo, los organozincs son más reactivos que los organostannanos y los organoboranos, lo que se correlaciona con tiempos de reacción más rápidos. La reacción lleva el nombre de Eiichi Negishi, co-ganador del Premio Nobel de Química 2010 por el descubrimiento y desarrollo de esta reacción, junto a Richard Heck y Akira Suzuki, por su trabajo sobre "acoplamientos cruzados catalizados por paladio en síntesis orgánica". Negishi y sus colaboradores investigaron originalmente el acoplamiento cruzado de reactivos de organoaluminio en 1976 empleando inicialmente Ni y Pd como catalizadores de metales de transición, pero notaron que el Ni resultó en la disminución de la estereoespecificidad mientras que el Pd no lo hacía. Transición de especies de organoaluminio a compuestos de organozinc Negishi y colaboradores informaron el uso de complejos de paladio en reacciones de acoplamiento de organozinc y llevaron a cabo estudios de métodos, eventualmente desarrollando las condiciones de reacción en las que se utilizan comúnmente en la actualidad.
From Wikipedia, the free encyclopedia
El acoplamiento de Negishi es una reacción de acoplamiento cruzado catalizada por metales de transición ampliamente utilizada. La reacción acopla halocarburos o triflatos con compuestos organometálicos de zinc, formando enlaces carbono-carbono (C-C) en el proceso. Generalmente se utiliza una especie de paladio (0) como catalizador metálico, aunque a veces se usa níquel.[1][2] Se puede emplear una variedad de catalizadores de níquel en estado de oxidación Ni0 o NiII en acoplamientos cruzados de Negishi como Ni(PPh3)4, Ni(acac)2, Ni(COD)2, etc.[3][4][5]

- El grupo saliente X suele ser cloruro, bromuro, o yoduro, pero también son factibles los grupos triflato and acetiloxi. Generalmente, si X = Cl conduce a reacciones lentas.
- El residuo orgánico R = alquenilo, arilo, alilo, alquinilo o propargilo.
- El haluro X' en el compuesto de organozinc puede ser cloruro, bromuro o yoduro y el residuo orgánico R' es alquenilo, arilo, alilo, alquilo, bencilo, homoalilo, and homopropargilo.
- El metal M en el catalizador es níquel o paladio.
- El ligando L en el catalizador puede ser trifenilfosfina, dppe, BINAP o chiraphos.
Los catalizadores de paladio en general tienen mayores rendimientos químicos y mayor tolerancia a los grupos funcionales.
El acoplamiento de Negishi encuentra un uso común en el campo de la síntesis total como un método para formar selectivamente enlaces C-C entre intermediarios sintéticos complejos. La reacción permite el acoplamiento de átomos de carbono sp3, sp2 y sp (ver hibridación orbital), lo que la hace algo inusual entre las reacciones de acoplamiento catalizadas por paladio. Los organozincs son sensibles a la humedad y al aire, por lo que el acoplamiento de Negishi debe realizarse en un ambiente libre de oxígeno y agua, un hecho que ha dificultado su uso en relación con otras reacciones de acoplamiento cruzado que requieren condiciones menos robustas (como la reacción de Suzuki). Sin embargo, los organozincs son más reactivos que los organostannanos y los organoboranos, lo que se correlaciona con tiempos de reacción más rápidos.
La reacción lleva el nombre de Eiichi Negishi, co-ganador del Premio Nobel de Química 2010 por el descubrimiento y desarrollo de esta reacción, junto a Richard Heck y Akira Suzuki, por su trabajo sobre "acoplamientos cruzados catalizados por paladio en síntesis orgánica".
Negishi y sus colaboradores investigaron originalmente el acoplamiento cruzado de reactivos de organoaluminio en 1976 empleando inicialmente Ni y Pd como catalizadores de metales de transición, pero notaron que el Ni resultó en la disminución de la estereoespecificidad mientras que el Pd no lo hacía.[6] Transición de especies de organoaluminio a compuestos de organozinc Negishi y colaboradores informaron el uso de complejos de paladio en reacciones de acoplamiento de organozinc y llevaron a cabo estudios de métodos, eventualmente desarrollando las condiciones de reacción en las que se utilizan comúnmente en la actualidad.[7]