Cianuro de calcio
El cianuro de calcio aparece como cristales o polvo blanco o polvo gris-negro (grado técnico). Al igual que otros cianuros similares, es muy tóxico por absorción cutánea a través de heridas abiertas, por ingestión y por inhalación. Es un compuesto inorgánico con la fórmula Ca(CN)2. Es un sólido blanco, aunque rara vez se observa en forma pura. Las muestras comerciales suelen ser negro-grisáceas. Es la sal de calcio del cianuro de hidrógeno. Se hidroliza fácilmente (incluso en aire húmedo) para liberar cianuro de hidrógeno.
From Wikipedia, the free encyclopedia
| Cianuro de calcio | ||
|---|---|---|
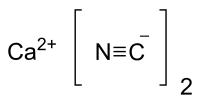 | ||
| Nombre IUPAC | ||
| Cianuro de calcio | ||
| General | ||
| Otros nombres | Dicianuro de calcio | |
| Fórmula estructural | Ca(CN)2 | |
| Fórmula molecular | CaC2N2 | |
| Identificadores | ||
| Número CAS | 592-01-8[1] | |
| ChemSpider | 11102 | |
| PubChem | 11590 | |
| UNII | 07DFJ2NTDD | |
|
[C-]#N.[C-]#N.[Ca+2]
| ||
| Propiedades físicas | ||
| Apariencia | blanco | |
| Densidad | 1853 kg/m³; 1,853 g/cm³ | |
| Masa molar | 92,113 g/mol | |
| Punto de fusión | 640 °C (913 K) | |
| Peligrosidad | ||
| SGA |
  | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El cianuro de calcio aparece como cristales o polvo blanco o polvo gris-negro (grado técnico).[2] Al igual que otros cianuros similares, es muy tóxico por absorción cutánea a través de heridas abiertas, por ingestión y por inhalación. Es un compuesto inorgánico con la fórmula Ca(CN)2. Es un sólido blanco, aunque rara vez se observa en forma pura. Las muestras comerciales suelen ser negro-grisáceas. Es la sal de calcio del cianuro de hidrógeno. Se hidroliza fácilmente (incluso en aire húmedo) para liberar cianuro de hidrógeno.[3]
El cianuro de calcio se puede preparar tratando el óxido de calcio (CaO) en polvo con ácido hidrociánico anhidro en ebullición en presencia de un acelerador como el amoníaco o el agua para minimizar la pérdida del ácido hidrociánico por polimerización:
También se puede preparar haciendo reaccionar ácido hidrociánico líquido con carburo de calcio. Alternativamente, el cianuro de calcio se puede preparar haciendo reaccionar ácido cianhídrico gas con cal viva (CaO) a altas temperaturas alrededor de 400 °C. A temperaturas más altas alrededor de 600 °C se forma cianimida de calcio en su lugar.[4] El material preparado a menudo está contaminado con derivados poliméricos de cianuro de hidrógeno, de ahí el color negro.
El cianuro de calcio se puede producir por azotación exotérmica de carburo de calcio a 1000 °C.[5] Surge como un intermediario en la producción de cianamida de calcio:
El cianuro de calcio también se produce en disolución acuosa haciendo reaccionar el ácido hidrociánico con hidróxido de calcio:[6]



