Hemeritrina
From Wikipedia, the free encyclopedia
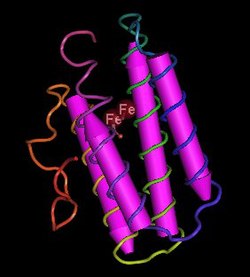
La hemeritrina (del griego haîma = sangre y erythrós = rojo) es una proteína oligomérica responsable del transporte de oxígeno (O2) en diversos filos de invertebrados marinos, en particular en sipuncúlidos, priapúlidos, braquiópodos, así como en anélidos del género Magelona. De forma más reciente, se ha identificado hemoemeritrina en bacterias metanotróficas de la especie Methylococcus capsulatus.[1]
La miohemeritrina es una proteína monomérica que se une al oxígeno que se localiza en los músculos de los invertebrados marinos. Tanto la hemeritrina como la miohemeritrina son prácticamente incoloras en su estado desoxigenado, pero adquieren una coloración violeta-rosada cuando se encuentran oxigenadas.
La hemeritrina no contiene el grupo hemo, a pesar de lo que podría sugerir su nombre. En realidad, las denominaciones de los principales transportadores biológicos de oxígeno, hemoglobina, hemocianina, y hemeritrina, no hacen referencia al grupo hemo característico de las globinas, presente únicamente en la hemoglobina), sino que derivan de la palabra griega que significa "sangre".








![{\displaystyle {\mathrm {O} {\vphantom {A}}_{\smash[{t}]{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a8c2c304a17b2fe1e4a79afb22d531d90f9c5ad1)
