Nitrato de bario
From Wikipedia, the free encyclopedia
| Nitrato de bario | ||
|---|---|---|
 | ||
 | ||
| General | ||
| Otros nombres | Dinitrato de bario | |
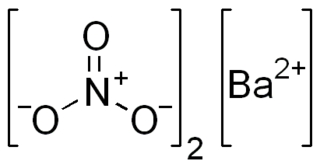
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 10022-31-8[1] | |
| ChEMBL | CHEMBL3184584 | |
| Propiedades físicas | ||
| Apariencia | cristales blancos | |
| Densidad | 3240 kg/m³; 3,24 g/cm³ | |
| Masa molar | 261,337 g/mol | |
| Punto de descomposición | 592 °C (865 K) | |
| Índice de refracción (nD) | 1.5659 | |
| Peligrosidad | ||
| NFPA 704 |
0
3
3
| |
| Frases R | R20/22 | |
| Frases S | S2 S28 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El nitrato de bario de fórmula química Ba(NO3)2 es una sal de compuesto de bario y el ion nitrato.
El nitrato de bario existe como un sólido blanco a temperatura ambiente. Es soluble en agua, y al igual que otros compuestos de bario solubles, es tóxico y debe ser manejado con cuidado. En la naturaleza está presente en un mineral raro, la nitrobarita .
El baratol es un compuesto explosivo de nitrato de bario, TNT y aglutinante; la alta densidad del nitrato de bario hace que el baratol también sea bastante denso. El nitrato de bario se mezcla con polvo de aluminio produce una pólvora destellante. Se mezcla con la termita para formar termate-TH3, que se utiliza en granadas de termita militares. También se utiliza en el proceso de fabricación de óxido de bario, en la industria de tubos de vacío y para dar fuego de color verde en pirotecnia.
Nitrato de bario se sintetiza en dos procesos. Uno consiste en disolver pequeños trozos de carbonato de bario en ácido nítrico, permitiendo todas las impurezas de hierro a precipitar, después se filtra, se evapora, y se cristaliza. El otro requiere la combinación de cloruro de bario con una solución calentada de nitrato de sodio, formándose cristales de nitrato de bario que precipitan.
