Síntesis de Kiliani-Fischer
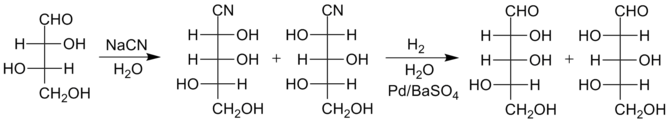
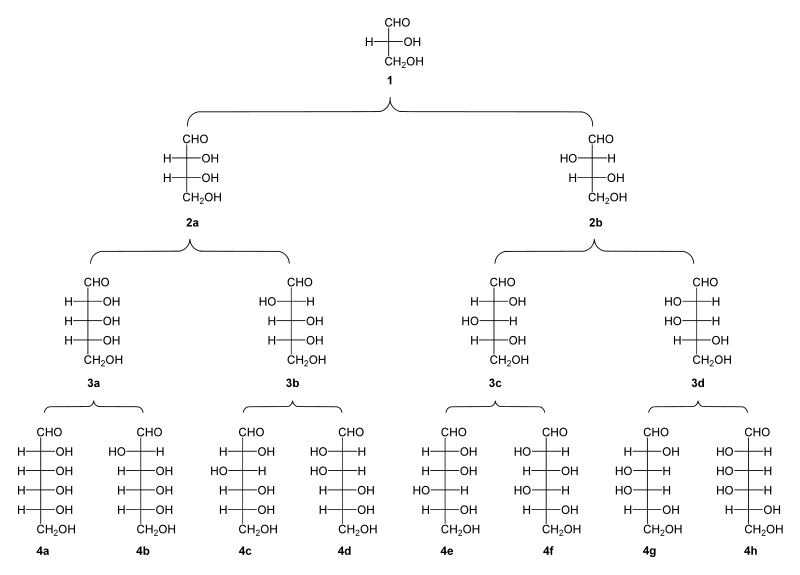
La síntesis de Kiliani-Fischer, nombrada así por los químicos Heinrich Kiliani y Hermann Emil Fischer, es un método para la síntesis de monosacáridos. Procede a través de la síntesis de hidrólisis de una cianhidrina del carbonilo de una aldosa, por la cual se alarga la cadena de carbono del carbohidrato precursor, conservándose así la estereoquímica en todos los carbonos quirales presentes anteriormente. El carbono quiral nuevo se produce con las dos estereoquímicas posibles, por lo que el producto de la síntesis de Fischer-Kiliani es una mezcla racémica de dos epímeros]. Por ejemplo, la D-arabinosa se convierte en una mezcla de D-glucosa y D-manosa.
From Wikipedia, the free encyclopedia
La síntesis de Kiliani-Fischer, nombrada así por los químicos Heinrich Kiliani y Hermann Emil Fischer, es un método para la síntesis de monosacáridos. Procede a través de la síntesis de hidrólisis de una cianhidrina del carbonilo de una aldosa, por la cual se alarga la cadena de carbono del carbohidrato precursor, conservándose así la estereoquímica en todos los carbonos quirales presentes anteriormente. El carbono quiral nuevo se produce con las dos estereoquímicas posibles, por lo que el producto de la síntesis de Fischer-Kiliani es una mezcla racémica de dos epímeros]. Por ejemplo, la D-arabinosa se convierte en una mezcla de D-glucosa y D-manosa.
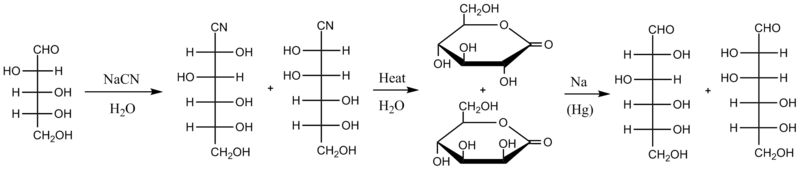
La versión original de la síntesis de Kiliani-Fischer procede a través de la cianhidrina y la lactona aldónica intermedia del ácido. El primer paso consiste en hacer reaccionar el azúcar a partir de cianuro acuoso (por lo general NaCN); el cianuro se somete a la adición nucleofílica en el grupo carbonilo del azúcar (mientras que los azúcares tienden a existir sobre todo como un hemiacetal cíclico piranósico, siempre están en equilibrio químico con su apertura de cadena forma aldehído o cetona, y en el caso de estos aldosas es la forma aldehído la que reacciona en esta síntesis). La cianhidrina resultante de esta adición se calienta en agua, que hidroliza el cianuro en un grupo ácido carboxílico, que rápidamente reacciona con un grupo hidroxilo intramolecular para formar una lactona más estable. Ahora hay dos lactonas diastereoisoméricas en la mezcla de reacción. Se pueden separar separados por cromatografía o partición en diferentes solventes) y luego la lactona deseada se reduce con una amalgama de sodio. Como se ilustra a continuación, la D-arabinosa se convierte en una mezcla de D-glucononitrilo y D manononitrilo, que luego se convierten en D-gluconolactona y D-manonolactone, se separan, y se reducen a D-glucosa o D-manosa. El rendimiento químico por este método tiende a ser alrededor del 30%.