Timidilato sintasa
From Wikipedia, the free encyclopedia
externos
| Timidilato sintasa | ||||
|---|---|---|---|---|
 Representación en cintas de la timidilato sintasa humana. En el sitio activo puede observarse el dUMP (en naranja) y el inhibidor Raltitrexed (en verde) análogo al N5,N10-metilenotetrahidrofolato. Fuente: PDB | ||||
| Estructuras disponibles | ||||
| PDB |
Lista de códigos PDB 3GH0
| |||
| Identificadores | ||||
| Nomenclatura |
Otros nombres 5,10-metilenotetrahidrofolato:dUMP C-metiltransferasa
| |||
| Símbolo | TS; HST422; MGC88736; TMS (HGNC: 12441) | |||
| Identificadores externos |
Bases de datos de enzimas
| |||
| Número EC | 2.1.1.45 | |||
| Número CAS | 9031-61-2 | |||
| Locus | Cr. 18 p11.32 | |||
| Estructura/Función proteica | ||||
| Tamaño | 312 (aminoácidos) | |||
| Peso molecular | 35.716 (Da) | |||
| Datos enzimáticos | ||||
| Actividad catalítica | Metiltransferasa | |||
| Información adicional | ||||
| Tipo de célula |
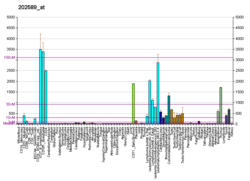 | |||
| Localización subcelular | Citosol | |||
| Ruta(s) | Síntesis de nucleótidos, Ciclo del folato | |||
| Ortólogos | ||||
| Especies |
| |||
| UniProt |
| |||
| RefSeq (proteína) NCBI |
| |||
| PubMed (Búsqueda) |
| |||
| PMC (Búsqueda) |
| |||

La proteína timidilato sintasa (TS) (EC 2.1.1.45)[1] es una enzima metiltransferasa homodimérica que cataliza la reacción de síntesis del timidilato (dTMP). Esta reacción es un paso fundamental en la formación de desoxitimidina 5'-trifosfato (dTTP), un metabolito necesario para la correcta síntesis y reparación del ácido desoxirribonucleico (ADN).[2]
En seres humanos, es el producto de la expresión del gen TYMS localizado en el brazo corto (p) del cromosoma 18.
Estructura primaria
La enzima timidilato sintasa es una proteína de aproximadamente 35,5KDa de peso. Está formada por la asociación de dos cadenas polipeptídicas idénticas (es un homodímero). Posee dos sitios activos, en los cuales se produce la trasformación del reactivo en producto, y dos sitios de unión a su cofactor, el N5,N10-metilenotetrahidrofolato.
En humanos, la traducción del gen TYMS genera cada una de las cadenas polipeptídicas que contienen 313 residuos inicialmente.[3]
| Residuos | Secuencia |
|---|---|
| 1-50 | MPVAGSELPR RPLPPAAQER DAEPRPPHGE LQYLGQIQHI LRCGVRKDDR |
| 51-100 | TGTGTLSVFG MQARYSLRDE FPLLTTKRVF WKGVLEELLW FIKGSTNAKE |
| 101-150 | LSSKGVKIWD ANGSRDFLDS LGFSTREEGD LGPVYGFQWR HFGAEYRDME |
| 151-200 | SDYSGQGVDQ LQRVIDTIKT NPDDRRIIMC AWNPRDLPLM ALPPCHALCQ |
| 201-250 | FYVVNSELSC QLYQRSGDMG LGVPFNIASY ALLTYMIAHI TGLKPGDFIH |
| 251-299 | TLGDAHIYLN HIEPLKIQLQ REPRPFPKLR ILRKVEKIDD FKAEDFQIEG |
| 300-313 | YNPHPTIKME MAV |
 En el proceso de maduración la Met1 es escindida produciéndose una cadena madura de 312 residuos con un residuo de Pro2 en el extremo aminoterminal.[4]
En el proceso de maduración la Met1 es escindida produciéndose una cadena madura de 312 residuos con un residuo de Pro2 en el extremo aminoterminal.[4] La Ser114 es fosforilada a fosfoserina.[4]
La Ser114 es fosforilada a fosfoserina.[4] La Cys195 se encuentra en el sitio activo y es esencial para la función de la enzima.[4] El 5-fluorodesoxiuridilato inhibe la enzima uniéndose a este residuo.[5]
La Cys195 se encuentra en el sitio activo y es esencial para la función de la enzima.[4] El 5-fluorodesoxiuridilato inhibe la enzima uniéndose a este residuo.[5]
Estructuras secundaria
Cada una de las cadenas polipeptídicas, también llamadas subunidades proteicas, adopta en el espacio patrones de plegamiento regionales que deben ser necesariamente conservados para el mantenimiento de la función enzimática de la proteína. En su estado nativo, que implica la conformación tridimensional donde la energía y tensión interna es mínima, la proteína posee 12 hélices α, 8 cadenas β y 4 giros.[4]
hélices α cadenas β giros
Cada subunidad está constituida por un solo dominio proteico, cuya disposición puede ser clasificada como α+β (las secciones con α hélices y hojas β se encuentran separadas entre sí, formando dos regiones bien definidas).[2]
Estructura terciaria
La proteína adopta una conformación espacial globular en la cual los aminoácidos con características polares se encuentran dispuestos mayormente en la superficie proteica, esto aumenta su solubilidad en el solvente acuoso intracelular e impide su precipitación.
Reacción catalizada
La enzima timidilato sintasa cataliza la reacción de transferencia de un grupo metilo desde el N5,N10-metilenotetrahidrofolato al desoxiuridilato (dUMP). Como producto de esta reacción se obtiene timidilato (dTMP) y 7,8-dihidrofolato, el cual se libera de la enzima y se recicla, por medio del ciclo del folato, nuevamente a N5,N10-metilenotetrahidrofolato.[2]
La reacción catalizada por la enzima timidilato sintasa es termodinámicamente favorable (ΔG<0) en condiciones fisiológicas y por ello no requiere el acoplamiento con otra reacción exergónica (como por ejemplo la hidrólisis de ATP) para ocurrir expontáneamente. Esto es ignorado en ciertas fuentes bibliográficas y por ello la enzima es llamada ocasionalmente, en forma errónea, "timidilato sintetasa".
Mecanismo de reacción
La transferencia del grupo metilo desde el N5,N10-metilenotetrahidrofolato al desoxiuridilato (dUMP) ocurre mediante un mecanismo en el cual intervienen numerosas reorganizaciones electrónicas. La Cys195 de la enzima posee una importancia fundamental en el mecanismo, debido a que la adición de su grupo sulfuro en el C5 del dUMP aumenta la reactividad del sustrato favoreciendo el avance de la reacción hacia la formación de productos.

