Tioacetal
Los tioacetales son los análogos de azufre de los acetales. Son preparados en una forma similar a los acetales: por reacción de un tiol con un aldehído:
- RSH + R'CHO → R'CH(OH)SR Tales reacciones típicamente emplean un catalizador, bien un ácido de Lewis o un ácido de Brønsted. Los ditioacetales generados a partir de aldehídos y 1,2-etanoditiol son útiles en síntesis orgánica:
- C2H4(SH)2 + R'CHO → R'CHS2C2H4 + H2O Aunque el carbono carbonílico de un aldehído es electrofílico, los derivados deprotonados de los ditioacetales presentan centros de carbono nucleofílico:
- R'CHS2C2H4 + R2NLi → R'CLiS2C2H4 + R2NH Nuevamente, esta reactividad es más comúnmente explotada en los 1,3-ditiolanos. La inversión de la polaridad entre R'(H)Cδ+Oδ- y R'CLi(SR)2 es referida como umpolung.
From Wikipedia, the free encyclopedia
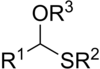

Los tioacetales son los análogos de azufre de los acetales. Son preparados en una forma similar a los acetales: por reacción de un tiol con un aldehído:[1]
- RSH + R'CHO → R'CH(OH)SR
Tales reacciones típicamente emplean un catalizador, bien un ácido de Lewis o un ácido de Brønsted.
Los ditioacetales generados a partir de aldehídos y 1,2-etanoditiol son útiles en síntesis orgánica:
- C2H4(SH)2 + R'CHO → R'CHS2C2H4 + H2O
Aunque el carbono carbonílico de un aldehído es electrofílico, los derivados deprotonados de los ditioacetales presentan centros de carbono nucleofílico:
- R'CHS2C2H4 + R2NLi → R'CLiS2C2H4 + R2NH
Nuevamente, esta reactividad es más comúnmente explotada en los 1,3-ditiolanos. La inversión de la polaridad entre R'(H)Cδ+Oδ- y R'CLi(SR)2 es referida como umpolung.