Acide dinitrobenzoïque
From Wikipedia, the free encyclopedia
L'acide dinitrobenzoïque est un composé aromatique de formule C7H4N2O6. Il est constitué d'un cycle benzénique substitué par un groupe carboxyle (acide benzoïque) et par deux groupes nitro. Il existe sous la forme de six isomères, en fonction de la position respective de ces groupes.
| Nom | Acide 2,3-dinitrobenzoïque | Acide 2,4-dinitrobenzoïque | Acide 2,5-dinitrobenzoïque | Acide 2,6-dinitrobenzoïque | Acide 3,4-dinitrobenzoïque | Acide 3,5-dinitrobenzoïque |
|---|---|---|---|---|---|---|
| Formule structurelle |  |
 |
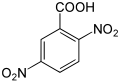 |
 |
 |
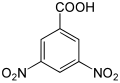 |
| Numéro CAS | ||||||
| PubChem | 283327 | 11880 | 11879 | 119206 | 10709 | 7433 |
| Formule brute | C7H4N2O6 | |||||
| Masse molaire | 212,12 g·mol−1 | |||||
| État | solide | |||||
| Apparence | poudre cristalline jaunâtre | |||||
| Point de fusion | 201 °C[1] | 179 à 183 °C[2] | 178 à 182 °C[3] | 202 °C (décomposition)[1] | 166 °C[4] | 204 à 206 °C[5] |
| PkA | 1,85[6] | 1,42[6] | 1,62[6] | 1,14[6] | 2,82[6] | 2,82[6] |
| Solubilité dans l'eau | 18,5 g·l-1 (25 °C)[2] | 6,73 g·l-1 (25 °C)[4] | ||||
| SGH | ||||||
| Phrase H et P | H315, H319 et H335 |
H315, H319 et H335 |
H302, H315, H319, H335 et H413 | |||
| P261 et P302+P352 P321, P305+P351+P338, P405 et P501 |
P261 et P305+P351+P338 |
P261 et P305+P351+P338 | ||||
Les acides dinitrobenzoïques sont des solides cristallins jaunâtres dont le point de fusion se situe entre 166 et 206 °C. Les acides dinitrobenzoïques ont une acidité plus élevée que l'acide benzoïque et les acides nitrobenzoïques en raison de l'effet -M des deux groupes nitro, en particulier lorsqu'ils sont adjacents au groupe carboxyle (position ortho). Les pkA varient ainsi entre 1,14 (isomère 2,6, en double position ortho) et 2,82, et sont globalement plus faibles que ceux des acides nitrobenzoïques (2,22-3,44), et bien plus faible que celui de l'acide benzoïque (4,20[6]).
