Ferrofluide
From Wikipedia, the free encyclopedia


Les ferrofluides sont des suspensions colloïdales de nanoparticules ferromagnétiques ou ferrimagnétiques d'une taille de l'ordre de 10 nanomètres dans un solvant ou de l'eau. Ces liquides deviennent magnétiques lors de l'application d'un champ magnétique extérieur tout en conservant leur stabilité colloïdale.
Une conséquence spectaculaire de cette propriété est que ces liquides sont attirés par les aimants ou les électroaimants, exactement comme un morceau de fer. Dans certains cas, si le champ magnétique est suffisant, ils se hérissent de pointes dont la topologie varie selon les paramètres du champ. Ces pointes sont peu rigides puisqu'elles se déforment si on les touche : la force exercée par le doigt l'emporte sur la cohésion du fluide. Ils ont des applications dans des domaines extrêmement variés.
Les ferrofluides sont le plus fréquemment composés de nanoparticules de magnétite (Fe3O4) ou de maghémite (γ-Fe2O3), qui sont tous deux des oxydes de fer.
Les ferrofluides sont apparus dans la deuxième moitié du XXe siècle. Ils n'existent pas à l'état naturel, il a donc fallu les synthétiser.
La première approche des fluides magnétiques (ou ferrofluides) a été réalisée par Gowin Knight au XVIIIe siècle, qui a préparé un fluide constitué de limaille de fer dans de l'eau[1]. Cependant, on ne peut parler d'une réelle synthèse de ferrofluide qu'à partir de 1963. C'est Stephen Papell[2] qui a effectué cette synthèse en mélangeant de la poudre de magnétite à du kérosène (essence) en présence d'acide oléique agissant comme tensioactif. Dans le but d'obtenir des nanoparticules, il a ensuite broyé pendant dix mois le liquide. L'objectif était de fabriquer un liquide de propulsion pour fusées en l'absence de gravité. Pour la première fois, un ferrofluide stable était créé.
Les travaux de Rosensweig ont amené à une amélioration du procédé, permettant l'obtention d'un ferrofluide plus concentré et magnétique. Il en est découlé une production industrielle et une commercialisation des ferrofluides, dans un premier temps essentiellement par l'entreprise Ferrofluidics.
Depuis, la recherche scientifique apporte régulièrement des avancées dans la synthèse des ferrofluides[3]. Par exemple, en 2019, des chercheurs de l'université du Massachusetts et de l'université de technologie chimique de Beijing ont réussi à créer un ferrofluide magnétique permanent qui conserve son magnétisme lorsque le champ magnétique extérieur est retiré[4].
Composition
Deux constituants entrent dans la composition d’un ferrofluide : des particules magnétiques solides et un liquide porteur dans lequel elles baignent.
- Les particules solides
Les oxydes magnétiques, principalement des particules de magnétite (Fe3O4), ferrite (MFe2O4 où M est un cation divalent : M=NiII, CoII, ZnII, BaII...) ou de maghémite (γ-Fe2O3) constituent une grande proportion des particules utilisées dans les ferrofluides. Pour les obtenir, on procède soit à un broyage, soit à une alcalinisation d’un mélange aqueux.
Les particules peuvent être aussi de type métallique (c'est-à-dire constituées par un métal au degré d'oxydation 0), par exemple le nickel, le cobalt, le fer, etc. L'avantage de ces particules est leur forte aimantation. Toutefois, leur rapide oxydation entraîne la diminution ou la perte de cette aimantation.
- Le liquide porteur
On en distingue deux types :
- les solvants organiques : essentiellement utilisés dans les applications commerciales, ils doivent avoir une grande stabilité à la température. Comme exemple, on peut citer : hydrocarbure aliphatique, diester carboxylique, huile de silicone, polyphényléther… .
- Les solvants polaires, principalement employés dans les applications médicales. L’eau et les alcools sont les exemples essentiels.
Un autre exemple de liquide porteur est le mercure, qui est un fluide métallique présentant des conductivités thermiques et électriques élevées. Cependant, le mercure est visqueux[5].
Synthèse
Les premières méthodes de synthèse consistaient à broyer des particules d'oxyde magnétique en présence du liquide porteur et d'un tensioactif. Ces méthodes étaient coûteuses en temps et en énergie et pas toujours reproductibles. Actuellement, de nombreux procédés existent pour synthétiser les nanoparticules magnétiques à la base des ferrofluides. La méthode de coprécipitation en milieu alcalin d'ions en solution aqueuse (par exemple par ajout d'ammoniaque NH3) a été mise au point par René Massart au début des années 1980 [6]. Cette méthode, facile à mettre en œuvre et reproductible, peut être résumée par la réaction chimique suivante :
M2+(aqu) + 2Fe3+(aqu) + 8OH−(aqu) = MFe2O4(s) + 4H2O (où M2+=Fe2+,Co2+ ... etc.)
Plus récemment des travaux ont été publiés sur la synthèse des nanoparticules magnétiques, en microémulsion, par décomposition thermique de complexes métalliques, par voie hydrothermale, par voie électrochimique, ou dans des canaux de microfluidique[7],[8]. Ces méthodes conduisent à des nanoparticules plus monodisperses ou avec des morphologies originales (nanoparticules sphériques, cubiques, en bâtonnet, en « fleur »...).
Stabilité colloïdale
Généralités
Pour pouvoir utiliser les propriétés spécifiques du ferrofluide, il doit être stable (il ne doit pas décanter, et doit rester homogène) même sous l'action d'un champ magnétique. Cette stabilité va dépendre de plusieurs paramètres tels que la taille des particules et certaines forces. Les forces auxquelles sont soumises les nanoparticules du ferrofluide sont :
- la force de Van der Waals, une force attractive à courte distance et de valeur proportionnelle à la dimension des particules ;
- la force magnétique, qui correspond à une interaction entre les pôles des nanoparticules. Elle est attractive lorsqu'un champ magnétique est appliqué ;
- la répulsion interparticulaire ;
- le terme entropique, correspondant à l'énergie d'agitation thermique ;
- la gravité.
Dans le cas où les forces attractives l'emportent sur les forces répulsives, le ferrofluide n'est plus stable. Cela entraine une séparation du liquide en plusieurs phases et/ou une précipitation des nanoparticules.
Cas des ferrofluides
Afin d'éviter ce phénomène la taille des nanoparticules doit être de l'ordre du nanomètre (de 5 à 15 nm) et elles doivent se repousser à courte distance. La répulsion interparticulaire est liée au choix du solvant et à l'état de la surface des nanoparticules qui peut éventuellement être modifié par l'adsorption d'agents dispersants tels que des molécules chargées, des tensioactifs ou des polymères. Ces agents dispersants jouent aussi sur les interactions entre la nanoparticule et le liquide porteur (propriétés de « solubilité » de la nanoparticule).
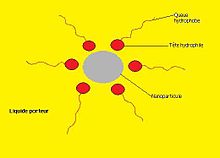
- Dans les milieux non polaires
- Les tensioactifs sont constitués d’une partie hydrophile (forte affinité avec la particule), et d’une partie hydrophobe (soluble dans le solvant).
- La partie hydrophile se fixe à la particule, la partie hydrophobe au solvant, ce qui permet de former l’interface liquide-solide, et donc de lier les deux composants. Un exemple typique de tensioactif utilisé est l'acide oléïque.
- Dans les milieux polaires
- Dans ce cas là, les nanoparticules doivent être chargées afin qu'elles puissent exercer les unes sur les autres des répulsions électrostatiques suffisamment fortes pour contrebalancer les forces attractives de Van-Der Walls et les interactions dipolaires magnétiques. Une première possibilité est de jouer sur le pH en se plaçant en dessous ou au-dessus du point isolectrique de la nanoparticule[9]. Ainsi les ferrofluides classiques de maghémite (γ-Fe2O3) ou de ferrite (MFe2O4) sont stables à pH<3 ou à pH>11. Pour obtenir de tels pH on ajoute à la suspension aqueuse des nanoparticules un acide tel que l'acide nitrique (HNO3) ou une base telle que l'hydroxyde de tétraméthylammonium ((CH3)4N+/OH−). La nature de la base ou de l'acide est également importante. Par exemple l'utilisation de bases telles que la soude (NaOH) ou l'ammoniaque (NH3) ne permet pas d'obtenir des ferrofluides stables. En effet la présence des contre-ions correspondant à ces bases (Na+, NH4+) écrante les charges de surface des nanoparticules, diminuant les répulsions électrostatiques et la stabilité colloïdale.
- Une deuxième possibilité consiste à adsorber à la surface une molécule ou un polymère chargé comme les anions citrate ou les polymères polyacrylate (PAA). Dans ce cas la stabilité colloïdale en fonction du pH dépend du pKa de l'espèce adsorbée. Par exemple avec les citrates, quand le pH est supérieur au pKa de cette molécule (environ 4), les molécules sont chargées négativement et confèrent cette charge aux nanoparticules qui sont alors stabilisées. On peut obtenir ainsi des ferrofluides stables en milieu neutre (pH=7).
- Une troisième possibilité est d'adsorber une bicouche de tensioactif (par exemple l'acide oléique) à la surface des nanoparticules. On met une première couche de tensioactif qui rend la particule hydrophobe. La deuxième couche permet à la particule de présenter des groupements polaires vers le solvant et donc d’être facilement solubilisée[5],[3]. Enfin il est à noter que la force ionique du milieu a également une importance sur la stabilité colloïdale en milieu polaire : une concentration en ions trop élevée ou la présence de cations divalents (par exemple Ca2+), écrante les charges de surface et diminue la stabilité colloïdale des nanoparticules.
Propriétés physiques
Propriétés magnétiques

Les ferrofluides possèdent de très fortes propriétés magnétiques :
- lorsque le fluide magnétique n'est soumis à aucun champ magnétique, les moments magnétiques portés par les nanoparticules sont orientés aléatoirement. L'aimantation totale du fluide est donc nulle.
- lorsque le ferrofluide est soumis à un champ magnétique, on observe une aimantation. Les moments des particules ont tendance à s'aligner avec le champ auquel elles sont soumises.
Les nanoparticules sont constituées d'un matériau qui peut être ferromagnétique ou ferrimagnétique mais elles ont un comportement global qui est habituellement superparamagnétique. La stabilité du ferrofluide est facilitée par le superparamagnétisme, puisque l'aimantation des nanoparticules change spontanément de sens avec l'agitation thermique, réduisant ainsi les interactions magnétiques entre nanoparticules. L'aimantation d'un ferrofluide à saturation est égale, à la dilution près, à celle des matériaux qui le compose. Par exemple, un ferrofluide à base de magnétite, concentré à 15 %, possède une aimantation de 52,5 kA/m (kiloampères par mètre, 103 A/m) à saturation[5],[3]. Cette aimantation ainsi que diverses propriétés caractéristiques du ferrofluide (susceptibilité magnétique, diamètre moyen et polydispersité des nanoparticules) peuvent être obtenues par mesure de sa courbe d'aimantation (c'est-à-dire de l'aimantation du ferrofluide, M, en fonction du champ magnétique extérieur appliqué, H). On utilise pour cela un magnétomètre vibrant ou un magnétomètre SQUID. L'ensemble de la courbe d'aimantation peut généralement être modélisé à l'aide de l'équation de Langevin.
Propriétés optiques
Les particules des ferrofluides ont des caractéristiques optiques particulières. Effectivement, ils sont biréfringents et dichroïques (propriété, lorsqu'il est éclairé par une lumière non polarisée, d'apparaitre bicolore lorsqu'on l'observe sous un certain angle par transparence) sous l'influence d'un champ magnétique. Ces caractéristiques sont beaucoup utilisées dans les applications des ferrofluides[5],[3].
Caractérisation
Les ferrofluides sont habituellement caractérisés par analyse chimique et spectrométrie d'absorption atomique (ce qui permet de doser le fer et ainsi de déterminer la concentration en nanoparticules), par diffraction des rayons X (afin de déterminer la nature des phases cristallines constituant les nanoparticules, mais aussi le diamètre moyen des nanoparticules), par magnétométrie vibrante ou magnétométrie SQUID (propriétés magnétiques, diamètre moyen et polydispersité des nanoparticules), par zêtamétrie (nature de la surface des nanoparticules), par diffusion dynamique de la lumière (DLS) (détermination du diamètre et de la polydispersité des nanoparticules) et par microscopie électronique à transmission (MET) (ce qui permet d'avoir une image directe des nanoparticules).