Hydroxyde de manganèse(II)
composé chimique
From Wikipedia, the free encyclopedia
L'hydroxyde de manganèse(II) est le composé inorganique de formule Mn(OH)2. C'est un solide blanc, bien que les échantillons noircissent rapidement en cas d'exposition à l'air à cause de l'oxydation. Il est peu soluble dans l'eau.

Dihydroxyde de manganèse, hydroxyde de manganèse, hydroxyde manganeux, pyrochroïte
| Hydroxyde de manganèse(II) | |
| |
| Identification | |
|---|---|
| Synonymes |
Dihydroxyde de manganèse, hydroxyde de manganèse, hydroxyde manganeux, pyrochroïte |
| No CAS | |
| No ECHA | 100.126.826 |
| No CE | 606-171-3 |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | solide blanc |
| Propriétés chimiques | |
| Formule | Mn(OH)2 |
| Masse molaire[1] | 88,952 7 ± 0,000 7 g/mol H 2,27 %, Mn 61,76 %, O 35,97 %, |
| Propriétés physiques | |
| T° fusion | se décompose |
| Solubilité | 0,00034 g/100 mL à 18 °C.[2] |
| Masse volumique | 3,258 g/cm3 |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'hydroxyde de manganèse(II) existe dans la nature, sous la forme du minéral appelé pyrochroïte[3].
Préparation et réactions
L'hydroxyde de manganèse(II) précipite sous forme solide lorsqu'un hydroxyde de métal alcalin est ajouté à une solution aqueuse de sel Mn2+[4] :
- Mn2+ + 2 NaOH → Mn(OH)2 + 2 Na+
L'hydroxyde de manganèse(II) s'oxyde rapidement dans l'air, comme l'indique le noircissement des échantillons.
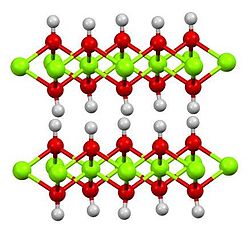
Le composé adopte la structure brucite, comme le font plusieurs di-hydroxydes de métal.