Importine
From Wikipedia, the free encyclopedia
Les importines sont une famille de protéines de type karyophérine[1] qui transportent des protéines de l'extérieur vers l'intérieur du noyau en se liant à des séquences particulières appelées signal de localisation nucléaire (NLS).
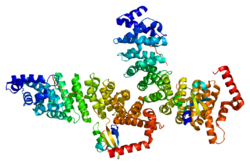
Importine α
Une importine possède deux sous-unités, l'importine α et l'importine β. Les importines β peuvent se lier à des protéines cibles et les transporter directement, ou bien former des hétérodimères avec une importine α. Dans ce cas, l'importine β assure les interactions avec le pore nucléaire tandis que l'importine α joue le rôle d'une protéine adaptatrice se liant au signal de localisation nucléaire de la protéine à transporter. Le trimère NLS–(importine α)–(importine β) se dissocie après liaison au complexe Ran–GTP à l'intérieur du noyau[2], les deux importines étant recyclées dans le cytoplasme pour un nouveau cycle.
Une partie importante de la sous-unité α, qui joue le rôle de protéine adaptatrice, est constituée de plusieurs répétitions armadillo arrangées en tandem. Ces répétitions peuvent s'empiler pour former une structure incurvée qui facilite la liaison à la séquence de localisation nucléaire spécifiques aux protéines à transporter. Le principal site de liaison au NLS se trouve à proximité de l'extrémité N-terminale, un site de liaison secondaire se trouvant à proximité de l'extrémité C-terminale. Outre les répétitions armadillo, l'importine α contient également une région N-terminale de 90 résidus d'acides aminés assurant la liaison à l'importine β et appelée domaine IBB[3]. C'est également un site d'autoinhibition, qui intervient par ailleurs dans la libération de la protéine transportée une fois que l'importine α se trouve dans le noyau[4].
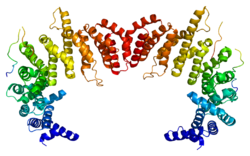
Importine β
Les importines β présentent la structure typique des protéines de la superfamille des karyophérines. Elle possèdent entre 18 et 20 répétitions HEAT en tandem, chacune de ces répétitions contenant deux hélices α antiparallèles liées par un coude et dont l'empilement constitue la structure générale de la protéine[5].
Afin de transporter vers l'intérieur du noyau la protéine à laquelle elle s'est liée, l'importine β doit se lier aux complexes des pores nucléaires. Elle y parvient à l'aide de liaisons faibles et transitoires avec les nucléoporines (en) au niveau de leurs motifs FG, ou Phe–Gly. Les analyses par cristallographie aux rayons X ont montré que ces motifs se lient à de poches hydrophobes peu profondes à la surface de l'importine β[6].
Cycle d'importation des protéines dans le noyau cellulaire
La principale fonction des importines est d'assurer la translocation des protéines possédant un signal de localisation nucléaire depuis le cytoplasme vers l'intérieur du noyau de la cellule à travers les complexes des pores nucléaires (NPC), ce qu'on appelle cycle d'import nucléaire des protéines.
Formation du complexe protéine-importine
Ce cycle commence par la liaison de la protéine à transporter. L'importine β monomérique seule peut réaliser cette étape, mais il faut généralement également une importine α formant un hétérodimère avec elle et jouant le rôle de protéine adaptatrice avec le NLS des protéines à transporter. Ce dernier est une séquence d'acides aminés basiques qui marque la protéine qui la porte comme devant être importée dans le noyau. Une protéine cible peut porter un ou deux de tels signaux, qui se lient aux sites de liaison principal et secondaire de l'importine α.
Importation du complexe dans le noyau
Une fois que la protéine à transporter est liée à l'importine, l'importine β interagit avec un complexe de port nucléaire afin de diffuser dans l'intérieur du noyau depuis le cytoplasme. La vitesse de diffusion dépend à la fois de la concentration en importine α dans le cytoplasme mais aussi de l'affinité de l'importine α pour la protéine à transporter. Une fois parvenu à l'intérieur du noyau, le complexe protéine–(importine α)–(importine β) interagit avec une protéine Ran, de la superfamille Ras (en), ce qui induit une modification conformationnelle de l'importine β et dissocie le complexe protéine–(importine α)–(importine β)–Ran en protéine–(importine α) d'une part et (importine β)–Ran–GTP d'autre part. L'importine β liée au Ran–GTP et est prête à être recyclée.
Dissociation du complexe protéine-importine-Ran-GTP
Le fragment protéine–(importine α) se dissocie à son tour au sein du noyau. Le mécanisme de cette dissociation fait intervenir le domaine IBB de la région N-terminale de l'importine α, qui contient une région autorégulatrice ressemblant au signal NLS. La dissociation d'avec l'importine β a pour effet de libérer ce site et de le faire entrer en compétition avec les protéines à transporter lorsqu'elles cherchent à se lier au site principal de liaison au NLS de l'importine α. C'est ce mécanisme qui assure la dissociation de la protéine transportée d'avec l'importine α. Dans certains cas, des facteurs de libération spécifiques tels que les nucléoporines (en) Nup2 et Nup50 (en) peuvent intervenir pour faciliter la dissociation de la protéine transportée[7].
Recyclage de l'importine
Enfin, l'importine α se lie à un complexe Ran-GTP/CAS (en) qui facilite sa sortie du noyau vers le cytoplasme. La protéines CAS appartient à la superfamille des karyophérines et constitue un facteur d'exportation nucléaire. Le complexe (importine β)–Ran-GTP retourne dans le cytoplasme, et le complexe Ran-GTP est hydrolysé par une protéine d'activation de l'activité GTPase (en) (GAP) pour donner le complexe Ran-GDP, ce qui libère l'importine β : c'est l'hydrolyse du GTP qui fournit l'énergie de l'ensemble du cycle d'import des protéines. Dans le noyau, un facteur d'échange de nucléotides à guanine (en) (GEF) charge la protéine Ran avec une molécule de GTP, qui est ensuite hydrolysée par une protéine d'activation de l'activité GTPase du cytoplasme : c'est l'activité GTPase de la protéine Ran qui assure le caractère bidirectionnel du transport des protéines à travers la membrane nucléaire[7].