Oxydation de Pinnick
From Wikipedia, the free encyclopedia
L'oxydation de Pinnick est une réaction de chimie organique consistant en une oxydation d'un aldéhyde en l'acide carboxylique correspondant. Elle est mise au point en 1981 par Harold Pinnick à partir des travaux de Lindgren et Kraus[1].
Le réactif oxydant est le chlorite de sodium et l'ajout au milieu réactionnel de 2-méthylbut-2-ène permet d'éviter la suroxydation du substrat[1]. La réaction est menée en présence d'un tampon de dihydrogénophosphate de sodium[1].
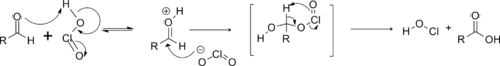
Le mécanisme réactionnel commence par la formation d'acide chloreux par réaction entre le chlorite et le dihydrogénophosphate[1].
L'acide chloreux protone ensuite l'aldéhyde, ce qui accentue l'électrophilie de son carbone fonctionnel, qui subit alors une attaque nucléophile par l'ion chlorite libéré. Un mécanisme concerté permet l'élimination de l'acide hypochloreux et la formation de l'acide carboxylique souhaité[1].
Réactions secondaires
L'acide hypochloreux créé lors de la réaction est responsable de deux réactions secondaires.
Dans la première, il réagit avec les ions chlorite pour former du dioxyde de chlore et des ions chlorure.
L'acide hypochloreux est un oxydant plus fort que l'ion chlorite[2]. Il va donc avoir tendance à oxyder d'autres fonctions du substrat que la fonction aldéhyde. Pour éviter cette suroxydation, on ajoute au milieu un excès de 2-méthylbut-2-ène[1].


