Propène
composé chimique
From Wikipedia, the free encyclopedia
Le propène, anciennement appelé « propylène », est un alcène de formule semi-développée CH2=CH-CH3. C'est un gaz sans odeur et sans couleur. Cet important composé de l'industrie pétrochimique est notamment utilisé pour la synthèse d'autres composés plus complexes tels le polypropylène.

| Propène | |
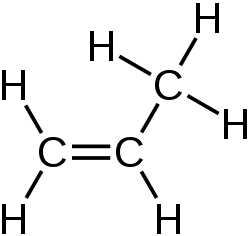  |
|
| Identification | |
|---|---|
| Nom UICPA | propène |
| Synonymes |
méthyléthylène |
| No CAS | |
| No ECHA | 100.003.693 |
| No CE | 204-062-1 |
| No RTECS | UC6740000 |
| PubChem | 8252 |
| ChEBI | 16052 |
| SMILES | |
| InChI | |
| Apparence | gaz comprimé liquéfié incolore[1]. |
| Propriétés chimiques | |
| Formule | C3H6 [Isomères] |
| Masse molaire[2] | 42,079 7 ± 0,002 8 g/mol C 85,63 %, H 14,37 %, |
| Propriétés physiques | |
| T° fusion | −185,24 °C[3] |
| T° ébullition | −47,69 °C[3] |
| Solubilité | 384 mg l−1 (eau, 20 °C)[4] |
| Masse volumique | 0,609 41 g cm−3 (liquide, −47,69 °C) 1,913 8 kg m−3 (gaz, 0 °C, 1 013 mbar)[4] |
| T° d'auto-inflammation | 485 °C[4] |
| Point d’éclair | −108 °C[4] |
| Limites d’explosivité dans l’air | 1,8–11,2 %vol[4] |
| Pression de vapeur saturante | 10,14 bar à 20 °C[4]
|
| Point critique | 4 594 kPa[6], 91,75 °C[7] |
| Thermochimie | |
| Cp | |
| PCS | 2 058,0 kJ mol−1 (25 °C, gaz)[8] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 9,73 ± 0,02 eV (gaz)[9] |
| Propriétés optiques | |
| Indice de réfraction | = 1,356 7[3] |
| Précautions | |
| SGH[10] | |
| H220 |
|
| SIMDUT[11] | |
   A, B1, D2B, |
|
| NFPA 704 | |
| Transport[4] | |
| Classification du CIRC | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[12] | |
| Écotoxicologie | |
| LogP | 1,77[13] |
| Seuil de l’odorat | bas : 23 ppm haut : 68 ppm[14] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Propriétés physico-chimiques
La principale caractéristique du propène est la réactivité de la double liaison qui en fait un bon réactif pour des réactions de polymérisation, d'addition et d'oxydation.
Production et synthèse
Une des principales sources pour le propène est la production d'éthylène où le propène constitue un sous-produit[15]. La fraction C3 issue de la production d'éthylène est isolée et subit une hydrogénation catalysée par du palladium pour éliminer le propyne et le propadiène. Deux étapes de purification sont nécessaires pour éliminer les oligomères et le méthane. À ce stade du procédé, le propène de qualité chimique (92-95 %mol de propène) est produit. Pour obtenir une qualité supérieure nécessaire aux réactions de polymérisation (99,5-99,8 %mol de propène), la séparation du propane est effectuée dans une colonne de rectification voire deux en fonction de l'équipement disponible[15].
Une autre source est le craquage dans les raffineries où la fraction C3-C4 est isolée via une colonne de distillation qui récupère la fraction C2 suivie d'un lavage à l'aide d'essence pour éliminer la fraction C5 et autres composés plus lourds. Une dernière rectification sépare le propène du propane[15].
Le propène peut être également synthétisé comme produit principal via la déshydrogénation du propane à l'aide d'un catalyseur en platine ou en chrome avec un rendement supérieur à 90 %[15]. Plusieurs procédés sont habituellement utilisés pour ce type de réaction : le procédé Oleflex, le procédé Houdry-Catofin, le procédé Phillips STAR et le procédé Linde[15].
Utilisation
Le propène est une des plus importantes matières premières dans l'industrie chimique[réf. nécessaire] et sert à la fabrication de nombreux produits chimiques : acroléine, acrylonitrile, acide acrylique[16], dérivés allyliques, polypropylène, propan-2-ol, 1,2-époxypropane et cumène. Le propylene est également un intermédiaire dans l'oxydation sélective au propane en une étape en acide acrylique[17],[18],[19].
Présence dans l'espace
La sonde Cassini, en utilisant son spectromètre infrarouge, a découvert du propène sur Titan, la plus grosse lune de Saturne[20].













