Réarrangement de Pummerer
From Wikipedia, the free encyclopedia
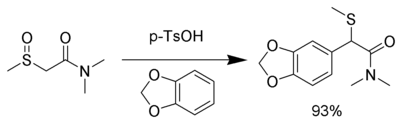
Le réarrangement de Pummerer est une réaction organique par laquelle un sulfoxyde d' alkyle se réarrange en un α- acyloxy - thioéther (mono thioacétal -ester) en présence d'anhydride acétique[1],[2],[3].

La stœchiométrie de la réaction est:
- RS(O)CHR'2 + Ac2O → RSC(OAc)R'2 + AcOH
La réaction a été découverte par le chimiste autrichien Rudolph Pummerer en 1909[4],[5].
Implémentation synthétique
L'anhydride acétique, l'anhydride trifluoroacétique et l'anhydride triflique ont été utilisés comme activateurs[6]. Outre les acétates, les nucléophiles les plus courants sont les arènes, les alcènes, les amides et les phénols.
L'utilisation de α-acylsulfoxydes et d'acide de Lewis, tels que TiCl4 et SnCl4, permet à la réaction de se dérouler à des températures plus basses (0 °C)[7].
Le chlorure de thionyle peut être utilisé à la place de l'anhydride acétique pour déclencher l'élimination pour former l'intermédiaire électrophile et fournir du chlorure comme nucléophile pour donner un α-chloro-thioéther[8] :

D'autres anhydrides et halogénures d'acyle peuvent donner des produits similaires. Les acides inorganiques peuvent également donner cette réaction. Ce produit peut être transformé en aldéhyde ou en cétone par hydrolyse[9].