Sulfate de césium
composé chimique
From Wikipedia, the free encyclopedia
Le sulfate de césium est un composé chimique de formule Cs2SO4. Il se présente comme une poudre blanche inodore très soluble dans l'eau, cristallisée dans le système orthorhombique avec le groupe d'espace Pmcn (no 62, position 5), qui connaît une transition de phase à 667 °C vers le groupe d'espace P3m1 (no 156) du système trigonal[4]. Il peut être obtenu en faisant réagir du carbonate de césium Cs2CO3 avec de l'acide sulfurique H2SO4 ou du bisulfate de césium CsHSO4[5]. On l'obtient également en traitant de la pollucite, une zéolithe de formule (Cs,Na)2Al2Si4O12·2H2O, avec de l'acide sulfurique[6].
| Sulfate de césium | |
 |
|
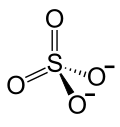
| Ions constituant le sulfate de césium | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.030.589 |
| No CE | 233-662-6 |
| No RTECS | FL0800000 |
| PubChem | 25137 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche inodore très soluble dans l'eau[1] |
| Propriétés chimiques | |
| Formule | Cs2SO4 |
| Masse molaire[2] | 361,874 ± 0,006 g/mol Cs 73,45 %, O 17,69 %, S 8,86 %, |
| Propriétés physiques | |
| T° fusion | 1 006 °C[1] |
| T° ébullition | 1 900 °C[3] |
| Solubilité | 1 820 g/L[3] à 25 °C |
| Masse volumique | 4,25 g/cm3[1] à 20 °C |
| Précautions | |
| SGH[1] | |
| H302, H361f, H373, P201, P264, P280, P312 et P301+P330+P331 |
|
| NFPA 704[3] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le sulfate de césium est utilisé dans les application de centrifugation en gradient de densité (en)[7], notamment en biotechnologie pour la caractérisation de protéines[8] et d'acides nucléiques[9].


