Synthèse de Williamson
From Wikipedia, the free encyclopedia

La synthèse de Williamson est une réaction organique formant un éther-oxyde à partir d'un halogénure organique et d'un alcool. Cette réaction a été développée par Alexander Williamson en 1850[2]. Cette réaction est importante dans l'histoire de la chimie organique car elle a aidé à prouver la structure des éther-oxydes.
Typiquement, cette réaction implique un ion alcoolate réagissant avec un halogénure d'alkyle, ou dérivé halogéné (R-X) par une SN2. L'alcoolate est formé par activation nucléophile à partir d'un alcool. Pour que cette synthèse ait un bon rendement, il faut que l'halogénure d'alkyle soit primaire. Le rendement décroit avec l'encombrement du R-X, car l'alcoolate est une base forte, donc même à froid les R-X secondaires et tertiaires subissent des Β-éliminations. Le mécanisme général est le suivant[3] :
Attention, il est faux de faire pointer la flèche de mécanisme provenant de l'oxygène directement sur un groupement R' qui représente tout le reste de la molécule, c'est pour cette raison que la flèche arrive sur un C intermédiaire. (Les atomes d'hydrogène ne sont pas représentés.)
Un exemple est la réaction entre l'éthanolate de sodium avec le chloroéthane pour former l'éther diéthylique et le chlorure de sodium :
- Na+C2H5O− + C2H5Cl → C2H5OC2H5 + Na+Cl−
Utilisation
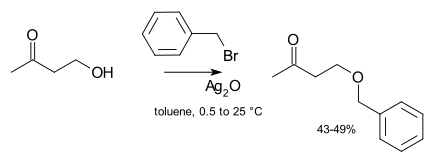
La synthèse de Williamson a un spectre d'utilisation assez large. Elle est largement utilisée à la fois en laboratoire et dans l'industrie et reste la méthode la plus simple et la plus populaire pour préparer des éther-oxydes. Les éthers aussi bien symétriques qu'asymétriques sont facilement préparés par cette synthèse. La réaction intramoléculaire chez les halogénohydrines en particulier donne des époxydes.
Dans le cas de la synthèse d'éthers asymétrique, il y a le choix entre deux types de réactifs (chaque côté pouvant être initialement l'halogénure ou l'alcool), on choisit en général selon la disponibilité du réactif, et sa réactivité. Il est également possible, de façon fréquente, d'utiliser la synthèse de Williamson à partir de deux alcools ; l'un d'eux est converti en halogénure (en utilisant généralement un tosylate), et les deux réactifs sont ensuite mis à réagir ensemble.
L'alcoolate peut être primaire, secondaire ou tertiaire. En revanche, l'agent alkyant doit être préférentiellement primaire. Les composés secondaires réagissent également, mais les tertiaires sont en général trop sujets à des réactions parasites pour être utiles. Le groupe partant est le plus souvent un halogénure ou un ester de sulfonate synthétisé pour le besoin de la réaction. Comme les conditions de la réaction sont plutôt dures, des groupes protecteurs sont souvent utilisés pour protéger les autres groupes sensibles des molécules utilisées (par exemple un autre groupe alcool, un groupe amine).