Trioxyde de xénon
composé chimique
From Wikipedia, the free encyclopedia
Le trioxyde de xénon est un composé instable du xénon à son état d'oxydation +6 qui se présente sous la forme d'un solide cristallin incolore[2]. C'est un agent oxydant très puissant qui libère lentement de l'oxygène et du xénon au contact de l'eau en une réaction qui s'accélère à la lumière du soleil. C'est également un explosif dangereux au contact des matières organiques, notamment de la cellulose[3],[4].

O 26,77 %, Xe 73,23 %,
| Trioxyde de xénon | |
 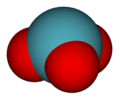 |
|
| Structure du trioxyde de xénon | |
| Identification | |
|---|---|
| No CAS | |
| Propriétés chimiques | |
| Formule | XeO3 |
| Masse molaire[1] | 179,291 ± 0,007 g/mol O 26,77 %, Xe 73,23 %, |
| Propriétés physiques | |
| T° fusion | 25 °C (explosion) |
| Solubilité | Soluble en donnant de l'acide xénique |
| Masse volumique | 4 550 kg·m-3 à 15 °C |
| Cristallographie | |
| Système cristallin | Orthorhombique |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Propriétés chimiques
Le trioxyde de xénon peut oxyder la plupart des substances oxydables, mais il réagit lentement, ce qui réduit sensiblement son intérêt comme agent oxydant[5]. En solution aqueuse, il forme une solution d'acide xénique :
- XeO3(aq) + H2O → H2XeO4 H+ + HXeO4−
Cette solution est stable à la température ambiante et ne possède pas le caractère explosif du trioxyde de xénon.
Propriétés physiques
Le tétrafluorure de xénon XeF4 donne par hydrolyse une solution à partir de laquelle on peut obtenir des critaux incolores de XeO3 par évaporation[6]. Ces cristaux sont orthorhombiques, avec a = 616,3 pm, b = 811,5 pm, c = 523,4 pm, et quatre molécules par maille élémentaire, avec une masse volumique de 4 550 kg/m3 [7] ; ils demeurent stables plusieurs jours à l'air sec, mais absorbent toute trace d'humidité pour donner une solution concentrée.
 |
 |
 |
| Modèle éclaté de XeO3 cristallisé. | Modèle compact de XeO3 cristallisé. | Coordinence du xénon dans le XeO3 cristallisé. |
