塩化アンモニウム
From Wikipedia, the free encyclopedia
塩化アンモニウム(えんかアンモニウム、ammonium chloride)は、化学式 NH4Cl、式量 53.50 [11]の塩。別名塩安(えんあん、Muriate)[11]。工業薬品JIS K1441-86、試薬JIS K8116-92、食品添加物[11]。

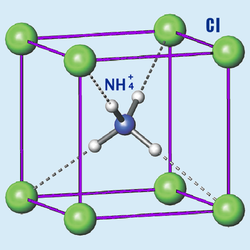 | |
 | |
| 物質名 | |
|---|---|
Ammonium chloride | |
別名 塩安 | |
| 識別情報 | |
| ECHA InfoCard | 100.031.976 |
| EC番号 |
|
| RTECS number |
|
CompTox Dashboard (EPA) |
|
| 性質 | |
| NH4Cl | |
| モル質量 | 53.49 g·mol−1 |
| 外観 | 白色または無色の結晶性固体、吸湿性 |
| 匂い | 無臭 |
| 密度 | 1.519 g/cm3[1] |
| 融点 | 338 °C (640 °F) |
| 337.6 °C で分解 1 atm[2] ΔdecompH | |
| 244 g/L (−15 °C) 294 g/L (0 °C) 383.0 g/L (25 °C) 454.4 g/L (40 °C) 740.8 g/L (100 °C)[4] | |
| 溶解度平衡 Ksp | 30.9 (395 g/L)[5] |
| 溶解度 | 液体アンモニア、ヒドラジンに溶ける、。アセトンにわずかに溶ける。ジエチルエーテル、酢酸エチルに溶けない。[2] |
| メタノールへの溶解度 | 32 g/kg (17 °C) 33.5 g/kg (19 °C) 35.4 g/kg (25 °C)[2] |
| エタノールへの溶解度 | 6 g/L (19 °C)[6] |
| グリセロールへの溶解度 | 97 g/kg[2] |
| 二酸化硫黄への溶解度 | 0.09 g/kg (0 °C) 0.031 g/kg (25 °C)[2] |
| 酢酸への溶解度 | 0.67 g/kg (16.6 °C)[2] |
| 蒸気圧 | 133.3 Pa (160.4 °C)[7] 6.5 kPa (250 °C) 33.5 kPa (300 °C)[6] |
| 酸解離定数 pKa | 9.24 |
| 磁化率 | −36.7·10−6 cm3/mol[8] |
| 屈折率 (nD) | 1.642 (20 °C)[2] |
| 熱化学 | |
| 標準モルエントロピー S⦵ | 94.85 J K−1 mol−1 [9] |
標準生成熱 (ΔfH⦵298) |
−314.55 kJ/mol[9] |
| 熱化学 | |
| 標準定圧モル比熱, Cp⦵ | 84.1 J/mol·K[6] |
| 標準モルエントロピー S⦵ | 94.56 J/mol·K[6] |
標準生成熱 (ΔfH⦵298) |
−314.43 kJ/mol[6] |
ギブズの 自由エネルギー (ΔfG⦵) |
−202.97 kJ/mol[6] |
| 薬理学 | |
| B05XA04 (WHO) G04BA01 (WHO) | |
| 危険性 | |
| GHS表示: | |
 [7] [7] | |
| Warning | |
| H302, H319[7] | |
| P305+P351+P338[7] | |
| NFPA 704(ファイア・ダイアモンド) | |
| 引火点 | 不燃性 |
| 致死量または濃度 (LD, LC) | |
半数致死量 LD50 |
1650 mg/kg (ラット, 経口) |
| NIOSH(米国の健康曝露限度): | |
PEL |
none[10] |
REL |
TWA 10 mg/m3 ST 20 mg/m3 (as fume)[10] |
IDLH |
N.D.[10] |
| 安全データシート (SDS) | ICSC 1051 |
古代ラテン語名のSal Ammoniac(アモンの塩)とも呼ばれるが、これはかつてエジプトのアモン神殿の近くから産出したことにちなむ。この名は、アンモニアの語源ともなった。
特徴
特性と用途
肥料として単独に、また化学肥料の原料としても広く用いられる[13]。工業用ではマンガン乾電池の電解液、亜鉛のメッキ、染料や染色助剤、光沢剤、電解質等、さらには医薬品原料や皮のなめし剤、火薬の原料にも使われる[11]。また、試薬としても用いられる[11]。
食品添加物としては、炭酸水素ナトリウム(重炭酸ソーダ)と併用して膨張剤として使われることが多い[11]。フィンランドなど北欧諸国で人気のあるサルミアッキ(リコリス菓子)というキャンディには塩化アンモニウムが使用されているため塩味とアンモニア臭がする。天然では、ダイオウイカなど一部のイカの仲間が浮力を得るために塩化アンモニウムを体内に保有している場合がある。特定のイカにある“えぐみ”はこのためである。
消石灰と混ぜ加熱しアンモニアを発生させる実験によく使われる。

![{\displaystyle {\mathrm {NH} {\vphantom {A}}_{\smash[{t}]{4}}{\vphantom {A}}^{+}{}\mathrel {\longrightleftharpoons } {}\mathrm {H} {\vphantom {A}}^{+}{}+{}\mathrm {NH} {\vphantom {A}}_{\smash[{t}]{3}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/9fcfc20d9d993cdb2e3d95f39b9e067a152efbcf)
![{\displaystyle {2\,\mathrm {NH} {\vphantom {A}}_{\smash[{t}]{4}}\mathrm {Cl} {}+{}\mathrm {Ca} (\mathrm {OH} ){\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {NH} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {CaCl} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}2\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/3270bae8a9f72639232be25772039b7c52f32e15)
![{\displaystyle {{\text{NH3}}{}+{}\mathrm {HCl} {}\mathrel {\longrightarrow } {}\mathrm {NH} {\vphantom {A}}_{\smash[{t}]{4}}\mathrm {Cl} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/d0855f2aaec528a09b3c53fbbc1d91ea92708def)
![{\displaystyle {{\text{NaCl}}{}+{}{\text{NH3}}{}+{}{\text{CO2}}{}+{}{\text{H2O}}{}\mathrel {\longrightarrow } {}{\text{NH4Cl}}{}+{}\mathrm {NaHCO} {\vphantom {A}}_{\smash[{t}]{3}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/214926d69e2e8b9ea8c7617799d28b6ddc90fd93)