オキソアニオン
From Wikipedia, the free encyclopedia
オキソアニオン(英: oxoanion)は、酸素を含む多原子陰イオン。オキシアニオン(英: oxyanion)とも表記される。いずれも酸素を意味する接頭辞 "oxo"、"oxy"と、陰イオンを意味する"anion"の組合せである。
化学式 AxOyz-(Aはある元素を指し、Oは酸素原子を指す)で表される化合物である。多くの元素がオキソアニオンを作ることができる[1]。単純なオキソアニオンの構造式はオクテット則により予想できる。縮合されたオキソアニオンの構造は AOn として、互いに辺や頂点を共有している多面体を単位にしてまとめられる。リン酸またはポリリン酸エステルである AMP、ADP、ATP は生物学において重要である。
単量体オキソアニオンの化学式 は元素Aの酸化数とその周期表での位置により定まる。第2周期元素の最大配位数は4であるが、この配位数では単量体オキソアニオンを作らない。代わりに、炭酸イオン や硝酸イオン は三角形型の平面構造であり、中心原子と酸素原子との間にπ結合をもつ。中心原子と酸素原子の大きさが近いとπ結合ができやすい。
第3周期元素のオキソアニオンは四面体型である。四面体形の SiO4 はカンラン石 [Mg,Fe]SiO4 で見つかるが、固体状態ではアニオンとカチオンが分離して存在しているわけではない。リン酸イオン PO43-、硫酸イオン SO42-、過塩素酸イオン ClO4- はさまざまな塩から見つかる。酸化数の低い元素のオキソアニオンの多くはオクテット則に従い、これにより化学式を求めることができる。たとえば、塩素原子(V)は2つの価電子を持つので、酸化物イオンから3つ電子対を受け取ることができる。イオンの電荷は+5 -3×2 = -1、よって化学式は ClO3- と求まる。VSEPR理論により予想されるこのイオンの構造は、3つの結合電子対と1つの非結合電子対をもった三角錐形構造である。同様に、塩素(III)のオキソアニオンの化学式は ClO2- と求まり、これは2つの非結合電子対と2つの結合電子対により折れ線形構造をしていると分かる。
| 酸化数 | 名称 | 化学式 | イメージ |
|---|---|---|---|
| +1 | 次亜塩素酸イオン |  | |
| +3 | 亜塩素酸イオン |  | |
| +5 | 塩素酸イオン |  | |
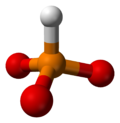
| +7 | 過塩素酸イオン |  |
第3周期以降の元素では配位数6が取れるようになるが、単独の八面体形オキソアニオンはあまりに高い電荷を持つため、知られていない。つまり、モリブデン(VI)は MoO66- を作ることはないが、四面体型のモリブデン酸イオン MoO42- は作ることができる。縮合されたモリブデン酸イオンからは MoO6 のユニットが見つかる。完全にプロトン化された八面体型オキソアニオンは、Sn(OH)62- や Sb(OH)6- などの化学種から見つかる。
縮合反応

水溶液において、大きな電荷を持つオキソアニオン同士の縮合反応が起こりうる。二クロム酸イオン Cr2O72- の生成はその例で、
この反応の駆動力は水分子生成による電荷密度の減少である。エントロピーが増加するとギブズ自由エネルギーが減少し、反応が促進されるが、上の反応ではエントロピーが減少 する。これは、塩基として働く単量体オキソアニオンと、その共役酸として働く縮合されたオキソアニオンの、酸塩基反応の例である。逆反応は加水分解反応であり、塩基として働く水分子が分解される。アデノシンリン酸塩のように、アニオンが特に大きな電荷を持つときは、さらなる縮合が起こることがある。
 |
 |
 |
| AMP | ADP | ATP |
ATP と ADP の変換は加水分解反応であり、生体系の重要なエネルギー源となる。
ケイ酸塩の生成は二酸化ケイ素がLux-Floodの定義での酸として働く、酸塩基反応である。




















![{\displaystyle K_{1}={\frac {[\mathrm {HCrO_{4}^{-}} ]}{[\mathrm {CrO_{4}^{2+}} ][\mathrm {H^{+}} ]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ba5183a196a004435f83e9cce025b6260ee6b4ed)

![{\displaystyle K_{2}={\frac {[\mathrm {Cr_{2}O_{7}^{2-}} ]}{[\mathrm {HCrO_{4}^{-}} ]^{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8247e0ecc828c99522eb74cce96893d4a0ca1f60)