リチウムアミド
From Wikipedia, the free encyclopedia
 | |
| 物質名 | |
|---|---|
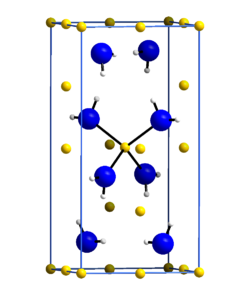
Lithium amide | |
別名 Lithium azanide | |
| 識別情報 | |
3D model (JSmol) |
|
| ChemSpider | |
| ECHA InfoCard | 100.029.062 |
PubChem CID |
|
| UNII | |
CompTox Dashboard (EPA) |
|
| |
| |
| 性質 | |
| LiNH 2 | |
| モル質量 | 22.96 g·mol−1 |
| 外観 | 白色の固体 |
| 密度 | 1.178 g/cm3 |
| 融点 | 375 °C (707 °F; 648 K) |
| 沸点 | 430 °C (806 °F; 703 K) 分解 |
| 反応する | |
| 溶解度 | エタノールにわずかに溶ける。アンモニアに溶けない。 |
| 熱化学 | |
| 標準生成熱 ΔfH |
−182 kJ/mol |
| 危険性 | |
| NFPA 704(ファイア・ダイアモンド) | |
リチウムアミドは、化学式「Li+NH2−」を持つ無機化合物。リチウムイオンとアミノアニオン(共役塩基アンモニア)で構成されている。水素化リチウムとアンモニアから製造される白色固体であり、常温で安定である。微量の加水分解により、発生するアンモニアの臭気を伴う。400℃以上でアンモニアの脱離を伴いながらリチウムイミドLi2NHに変化する。有機溶媒への溶解性は低いが、液体アンモニアには可溶である。水と接触して水酸化リチウムとアンモニアを生成する。アミンのアルキル化、カルバニオン生成試薬、パラジウム触媒によるアミノ化などに利用されている[1]。水素化リチウムとリチウムイミドはどちらも水素貯蔵材料として期待されている。
