Methylenblau
organische Verbindung, Farbstoff, Arzneimittel
From Wikipedia, the free encyclopedia
Methylenblau (Synonym: Methylthioniniumchlorid, lateinisch Methylenum caeruleum, systematische Bezeichnung nach Colour Index C.I. Basic Blue 9) ist ein Phenothiazin-Derivat. Der kationische Farbstoff wird in der Chemie, Medizin und Färbetechnik verwendet.

| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
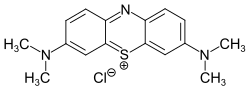 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Methylthioniniumchlorid[1] | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C16H18ClN3S | |||||||||||||||||||||
| Kurzbeschreibung |
dunkelgrüne, glänzende Kristalle[3] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 319,86 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Als reiner Farbstoff erscheint Methylenblau dunkelgrün, als Pulver oder Kristalle. Das im Handel auch übliche Methylenblau als Doppelsalz mit Zinkchlorid ist ein braunes Pulver. Die Weltgesundheitsorganisation führt Methylenblau als Arzneimittel zur Behandlung der Methämoglobinämie in der Liste der unentbehrlichen Arzneimittel.[7] Methylenblau war 1891 das erste vollsynthetische Arzneimittel.[8]
Geschichte

Methylenblau wurde erstmals 1876 von dem Chemiker Heinrich Caro bei der BASF synthetisiert.[9] Ein Jahr später erhielt die BASF für Methylenblau das erste Deutsche Reichspatent für einen Teerfarbstoff.[10][9] Paul Ehrlich verwendete Methylenblau 1887 zur Färbung lebender Nervenzellen (Vitalfärbung).[11] Im Jahr 1891 verwendeten Ehrlich und Paul Guttmann Methylenblau zur Behandlung der Malaria.[12][9] Er erkannte, dass Methylenblau sich an manche Erreger band, sie anfärbte und im Wachstum hemmte. In den 1890ern wurde Methylenblau zur Markierung der Medikamenteneinnahme von Patienten in der Psychiatrie verwendet, bei der eine antipsychotische Wirkung des Methylenblaus entdeckt wurde.[13][14] Da das Reduktionspotential des Methylenblaus dem des Sauerstoffs ähnelt und es in der Elektronentransportkette der Atmung reduziert werden kann, wurde Methylenblau zur Behandlung von Cyanidvergiftungen 1926 von Bo Sahlin und erstmals erfolgreich 1933 von Matilda Moldenhauer Brooks (und auch gegen Kohlenmonoxid-Vergiftungen) eingesetzt.[15][16][17] Im Jahr 1928 wurde die Photoinaktivierung bei Lichtbestrahlung in Anwesenheit von Methylenblau bei Bakterien[18][19] und 1933 bei Viren gezeigt.[20][19] In den 1930er Jahren wurde Methylenblau zur Therapie der Methämoglobinämie[21] und wegen seiner antibiotischen und antihelminthischen Eigenschaften verwendet.[22] Die Forschung an Phenothiazin-Derivaten führte in den 1940er Jahren zur Entdeckung von Promethazin, Promazin und 1951 letztlich Chlorpromazins als erstem wirksamen Neuroleptikum zur Behandlung der Schizophrenie und der Manie,[23][24][22] zur Entdeckung mancher Antihistamine wie Promethazin, des Malariamittels Chloroquin[25] und der trizyklischen Antidepressiva.[14]
Eigenschaften
Methylenblau ist ein dunkelgrünes Pulver mit bronzefarbenem Glanz, das in Wasser oder Ethanol gelöst einen blauen Farbstoff ergibt.[2] Es absorbiert sichtbares Licht im Bereich von circa 530 bis 700 nm mit einem Absorptionsmaximum bei 665 nm.[26][27] Das Maximum bei 292 nm stammt vom aromatischen Ringsystem, das Maximum bei 612 nm vom insgesamt zweifach positiv geladenen Methylenblau-Dimer und das Maximum bei 665 nm entstammt dem π–π*-Übergang (2,48 eV).[27] Weil Methylenblau Licht im blauen Wellenlängenbereich (zwischen 460 und 490 nm) nicht absorbiert, sondern reflektiert, erscheint es blau. Methylenblau fluoresziert sichtbar im Nahinfrarot-Bereich mit einer Quantenausbeute von 0,52 und einem Maximum bei 686 nm, was einer Stokes-Verschiebung von 21 nm zur Anregungswellenlänge 665 nm entspricht.[28]
| Molekül (MB = Methylenblau)[29] | Absorptionsmaximum | Extinktionskoeffizient (dm3/mol·cm) |
|---|---|---|
| MB+ (Lösung) | 664 | 95000 |
| MBH2+ (Lösung) | 741 | 76000 |
| (MB+)2 (Lösung) | 605 | 132000 |
| (MB+)3 (Lösung) | 580 | 110000 |
| MB+ (an Ton adsorbiert) | 673 | 116000 |
| MBH2+ (an Ton adsorbiert) | 763 | 86000 |
| (MB+)2 (an Ton adsorbiert) | 596 | 80000 |
| (MB+)3 (an Ton adsorbiert) | 570 | 114000 |
Es hat eine berechnete Van-der-Waals-Oberfläche von 387,92 Å2, eine polare Oberfläche von 43,91 Å2, ein elektrisches Dipolmoment von 11,22 D und ein Van-der-Waals-Volumen von 261,01 Å3.[30] Der kristalline Feststoff zeigt eine ausgeprägte Tendenz zur Hydratbildung. So lassen sich mit einem Pentahydrat, einem 2,2–2,3–Hydrat, zwei polymorphen Dihydraten und einem Monohydrat fünf verschiedene Hydratformen differenzieren.[31] Die Löslichkeit von Methylenblau ist folgend gereiht: Ethylacetat << Aceton << Ethanol < Wasser < Methanol und 2-Propanol.[32]
- Methylenblau-Lösung
- Methylenblau-Pulver
- Methylenblau-Kristalle
- Methylenblau-Kristalle in Originalgefäß
Herstellung
Methylenblau wird in mehreren Schritten aus N,N-Dimethyl-p-phenylendiamin unter Zusatz von Dichromat als Oxidationsmittel sowie der Addition von N,N-Dimethylanilin hergestellt. Abschließend muss es zum Indamin oxidiert werden, wobei sich Bindschedlers Grün bildet. Dieses wird in Gegenwart von Kupfersulfat mit Schwefelwasserstoff cyclisiert.
Alternativ kann Methylenblau durch Oxidation von 4-Aminodimethylanilin in Gegenwart von Natriumthiosulfat zur Chinondiiminothiosulfonsäure, anschließender Reaktion mit Dimethylanilin, Oxidation zum Indamin und Cyclisierung zum Thiazin hergestellt werden.[33]
Die Synthese von Methylenblau lässt sich in fünf Schritte unterteilen. Dabei wird N,N-Dimethylanilin vorgelegt und mit Salzsäure und Natriumnitrit versetzt. Dabei entsteht p-Nitroso-N,N-dimethylanilin. Durch Zugabe von Zink wird die entstandene Nitrosogruppe zu einem Amin reduziert. Anschließend reagiert das Produkt der Reduktion p-Amino-N,N-dimethylanilin unter Zugabe von konzentrierter Schwefelsäure und Thioschwefelsäure zu der Thiosulfonsäure von p-Amino-N,N-dimethylanilin. Bei der erneuten Zugabe von konzentrierter Schwefelsäure und der Zugabe eines weiteren Äquivalents von N,N-Dimethylanilins entsteht die Thiosulfonsäure von Bindschedlers Grün. Dies geschieht in einer oxidativen Kupplungsreaktion. Aus der Thiosulfonsäure von Bindschedlers Grün entsteht durch Zugabe von Mangandioxid das gewünschte Produkt Methylenblau.[34]
Gereiftes Methylenblau
In der Histologie wird gelegentlich „gereiftes“ oder „polychromes“ Methylenblau verwendet.[35] Dabei handelt es sich um spontane Demethylierungen zu Tri-, Di-, Mono- und unmethylierten Reaktionsprodukten, die respektive als Azur B, Azur A, Azur C und Thionin bezeichnet werden.[36]
Verwendung als Färbemittel



In Wasser löst sich Methylenblau gut, selbst geringe Mengen bewirken eine sichtbare Färbung des Wassers. Es wird zur Färbung von Seide, Holz, Baumwolle und Leder verwendet.[37][27] Weltweit wurde im Jahr 2023 Methylenblau im Wert von etwa 7,7 Milliarden US-Dollar umgesetzt.[27] Der größte Teil wurde 2024 im Gesundheitswesen, gefolgt von der Aquakultur, Laboren und der Textilindustrie verwendet.[38]
Histologie
In der Histologie wurde es 1885 erstmals durch Paul Ehrlich zur selektiven Färbung bestimmter Gewebearten (besonders der grauen Substanz im peripheren Nervensystem) verwendet. Die Färbung mit Methylenblau ist am lebenden Organismus möglich (Vitalfärbung), daher zählt man es zu den Vitalfarbstoffen. Es färbt vor allem Zellkerne, genauer gesagt die Nukleinsäuren darin. Die bakteriologische Verwendung des alkalischen Methylenblaus wird auch als Loeffler-Färbung[39] (nach Friedrich Loeffler) bezeichnet. Methylenblau ist Bestandteil vieler histologischer Färbungen wie der Giemsa-Färbung, der Romanowsky-Färbung, der Ziehl-Neelsen-Färbung, der May-Grünwald-Färbung, der Pappenheim-Färbung, der Field-Färbung, der Wright-Färbung, der Neisser-Färbung, der Leishman-Färbung, der Jenner-Färbung, der Jaswant-Singh-Bhattacharji-Färbung, der Kinyoun-Färbung und der Moeller-Färbung.
Biochemie
In der Biochemie wird Methylenblau zum Färben von DNA und RNA in Gelen und auf Membranen nach dem Blotten verwendet.[40] Zwar ist Methylenblau nicht so sensitiv wie andere DNA-Farbstoffe (wie Ethidiumbromid), dafür aber weniger toxisch und es interkaliert nicht in die Nukleinsäure-Ketten. Methylenblau ist permeabel für Biomembranen (auch als membrangängig bezeichnet) und kann bis ins Innere der Mitochondrien diffundieren.[19] Daneben wird es zur Virusinaktivierung per Photoinaktivierung[41] und zum Zählen von Viren im Plaque-Assay verwendet.[42] In der Mikrobiologie wird es im Eosin-Methylen-Blau-Agar[43] und zum Nachweis Reduktase-bildender Bakterien als Methylenblaumilch eingesetzt.[44]
Weiterhin wird Methylenblau als Redoxmediator eingesetzt. Das Halbwertspotential E0' beträgt +0,011 mV.[45][46] Unter reduzierenden Bedingungen wird Methylenblau zum farblosen Leukomethylenblau (LMB) reduziert.[47] In der Elektronentransportkette in Mitochondrien reagiert Methylenblau direkt mit NADH, NADPH und FADH2.[48] Weiterhin kann Methylenblau Elektronen in der Atmungskette von NADH am Komplex I auf Cytochrom c übertragen und Teile der Atmungskette überspringen.[19] Es bindet an Tubulin und hemmt die Bildung von Mikrotubuli im Zytoskelett.[49] Ebenso hemmt Methylenblau die lösliche Guanylylcyclase und die nachfolgende Bildung von cyclischem Guanosinmonophosphat (cGMP) als sekundärem Botenstoff, und verhindert damit die vasodilatierende Wirkung von NO.[50] Darüber hinaus aktiviert Methylenblau den Nrf2-Signalweg zum Abbau von reaktiven oxidativen Spezies zur Minderung von oxidativem Stress.[51]
Chemie

Methylenblau wird als Redoxindikator benutzt.[52][53] Es ist ein guter Wasserstoff-Akzeptor, der Alkohole in Gegenwart von Platin zu Aldehyden oxidiert. Dabei entfärbt sich die Lösung, da Methylenblau zum farblosen Leukomethylenblau reduziert wird.[54][52] Eine analoge Reaktion lässt sich auch mit Glucose und Luftsauerstoff als Blue-Bottle-Experiment durchführen.[55] Eine entsprechende Redoxreaktion läuft ab, wenn man zu einer Methylenblaulösung verdünnte Schwefelsäure und etwas Zinkpulver gibt. Methylenblau wird zur farblosen Leukoform reduziert. Die farblose Lösung wird nach Schütteln an der Luft wieder blau, weil die Leukoform vom Luftsauerstoff wieder zum Methylenblau oxidiert wird. In der Analytischen Chemie wird Methylenblau in der Bestimmung von Aniontensiden nach der Longwell-Manience-Methode und bei der Epton-Titration verwendet. Ebenso wird es zum Nachweis von Schwefelwasserstoff (im Konzentrationsbereich 0,02 – 1,50 mg/L, entsprechend 20 ppb – 1,5 ppm) mit Dimethyl-p-phenylendiamin und Eisen(III) bei pH 0,4 – 0,7 per Photometrie eingesetzt.[56] Hierbei ist Methylenblau allerdings kein Reagenz, sondern wird bei der Reaktion gebildet.[56] Reduktionsmittel wie Ascorbinsäure sind beim Sulfidnachweis Störsubstanzen, da sie Methylenblau zum farblosen Leukomethylenblau reduzieren.[52] In der Lebensmittelchemie wird Methylenblau zum Nachweis des Alters von Milch verwendet, da frische Milch noch ausreichend Sauerstoff enthält, um Methylenblau in der oxidierten blauen Form zu halten und ältere Milch es zu Leukomethylenblau reduziert.[57][58]
Geologie
In der Geologie dient die Methylenblau-Methode zur Bestimmung des Smektitgehalts in Tonmineralien.[59][60] Es stellt damit ein wichtiges Verfahren zur Qualitätskontrolle in vielen Industriezweigen dar. In der Abwasseranalytik wird eine Methylenblauprobe zur Bestimmung der Fäulnisfähigkeit herangezogen. Mit Hilfe der Methylenblauprobe kann der Nachweis geführt werden, ob bzw. in welchem Maße der Ablauf einer Kläranlage noch fäulnisfähige Stoffe enthält. Methylenblau ist ein Redoxindikator und entfärbt sich bei absolutem Luftabschluss in dem Maße, in dem anaerobe Verhältnisse (H2S-Bildung) überhandnehmen. Es wird die Zeit bis zur Entfärbung des der Probe zugesetzten Farbstoffes bestimmt.
In der Abwasseranalytik wird Methylenblau zur Bestimmung der Konzentration an anionischen Tensiden in Wasser verwendet (MBAS-Assay).[61][62] Methylenblau wird zur Bestimmung der verbliebenen Kapazität von Aktivkohlefiltern verwendet, da es ähnlich wie Medikamente und Pestizide daran bindet. Ebenso wird versucht, Methylenblau aus Abwässern zu adsorbieren.[63][64][65]
Medizinische Verwendung

In der Medizin ist Methylenblau in erster Linie bei der Behandlung der Methämoglobinurie ein Antidot gegen Nitrit- und Anilinvergiftungen, Vergiftungen mit manchen Arzneistoffen, Toxinen oder Ackerbohnen.[66] Methylenblau beschleunigt bei der entstehenden Methämoglobinämie die Rückumwandlung von Methämoglobin zu funktionsfähigem Hämoglobin von mehreren Stunden auf wenige Minuten.[67][68] Bei hohen Dosen an Methylenblau entsteht allerdings der umgekehrte Effekt und es erzeugt eine Methämoglobinämie.[68] Im Körper des Patienten wird Methylenblau zu Leukomethylenblau reduziert, das wiederum bei der Methämoglobinämie die Eisenionen Fe3+ zu Fe2+ reduziert, wodurch aus Methämoglobin wieder Hämoglobin entsteht und es wieder funktionsfähig wird.[69] Dabei wird es intravenös verabreicht.[57]
Ebenso wird Methylenblau als Antidot bei Cyanid- und Akee-Vergiftungen verwendet,[27][70] wobei Methylenblau bei Cyanid-Vergiftungen nicht mehr empfohlen wird.[57] Weiter wird es noch als Antiseptikum,[71] zur Bekämpfung von Malaria (seit über einem Jahrhundert[72]),[73][74][75] zur Behandlung Ifosfamid-induzierter Enzephalopathie[76][77] und zu Diagnosezwecken eingesetzt. Methylenblau wird als Enzymhemmer der löslichen Guanylylcyclase und damit beim septischen Schock und beim vasoplegischen Syndrom eingesetzt,[78] weil es die Dauer der Beatmung, der Gabe von Vasopressoren und den Aufenthalt in der Intensivstation verkürzt.[79][80][81]
Methylenblau wird als Placebo eingesetzt, nachdem den Patienten gesagt wurde, dass sich ihr Urin durch die Behandlung blau färben würde und dies ein Anzeichen für eine Verbesserung der Krankheit sei.[82] Die Farbigkeit des Urins nach Methylenblau-Gabe erschwert klinische Studien mit Methylenblau als Medikament in höheren Dosen, da die Versuchsteilnehmer an ihrem Urin sehen können, wer Methylenblau erhalten hatte. Daher erhalten die Probanden der Placebogruppe bei klinischen Studien mit Methylenblau manchmal eine so niedrige Dosis an Methylenblau, das gerade noch eine Blaufärbung des Urins erfolgt und somit eine Unterscheidung anhand des Urins schwieriger wird.[83] Allerdings ist bei den niedrigen Dosen eine Wirkung des Methylenblaus in der Placebogruppe nicht ausgeschlossen.[84]
Als Färbemittel wird es am lebenden Menschen bei der Nah-Infrarot-Darstellung der Harnröhre, zur Identifikation des Parathymus, von Pankreaskrebs, Brustkrebs und Krebs in Lymphknotenbiopsien[85][86] sowie beim Auffinden von Lymphknoten verwendet.[28] Methylenblau erhöht die Photosensibilität und wird in der photodynamischen Therapie zur Behandlung von Hautkrebs und Darmkrebs eingesetzt.[87] Bei einem Plasmaaustausch wird es in Verbindung mit Licht zur Photoinaktivierung behüllter Viren in Blutplasma verwendet.[88][89]
In der Tiermedizin, Aquaristik und Aquakultur wird es, teilweise zusammen mit Malachitgrün, als Mittel gegen einzellige Hautparasiten der Fische im Süßwasser eingesetzt wie Ichthyophthirius (erzeugen die Weißpünktchenkrankheit), Ichthyobodo (Costia), Heteropolaria, Chilodonella (erzeugen die Chilodonelliasis), Tetrahymena, Trichodina, Glossatella und im Salzwasser wie Cryptocaryon, Brooklynella und Uronema. Ebenso wird es bei Fischen als Bakterizid und Fungizid verwendet, unter anderem gegen Saprolegnia (erzeugen Saprolegniasis).[90][91]
Medizinische Forschung
Weiterhin wird der Farbstoff auf seine Eignung zur Behandlung von chronischen Schmerzen des unteren Rückens untersucht.[92] Methylenblau wird als lokales Analgetikum untersucht.[93][94]
Methylenblau wird zur Therapie verschiedener neurodegenerativer Erkrankungen untersucht, da es im Laborversuch die Aggregation von Tau-Proteinen hemmt[95][96] und die Funktion der Mitochondrien verbessert (Sauerstoffverbrauch und ATP-Erzeugung).[97][98] Weiterhin wird es zur Behandlung der Alzheimer-Krankheit,[99] von Depression, Angstzuständen und zur Neuroprotektion untersucht.[84][100][8][9]
Nebenwirkungen
| Kardiovaskulär[101][102] | Zentrales Nervensystem[101][102] | Dermatologisch[101][102] | Gastrointestinal[101][102] | Urologisch[101][102] | Hämatologisch[101][102] |
|---|---|---|---|---|---|
| • Bluthochdruck[103] • Brustschmerz[103] • Atemnot[103] |
• Schwindel • Geistige Verwirrung • Kopfschmerzen • Fieber |
• Verfärbung der Haut • Nekrose der Injektionsstelle |
• Verfärbung des Stuhls • Übelkeit[103] • Erbrechen[103] • Unterleibsschmerzen |
• Verfärbung des Urins (Dosen über 80 µg) • Blasenreizung |
• Hämolyse[103] und Anämie • Methämoglobinämie[103] |
Methylenblau wirkt in bestimmten Konzentrationen neurotoxisch.[104][105][103] Gaben von über 5 mg/kg Körpergewicht können im Menschen ein lebensgefährliches Serotonin-Syndrom auslösen.[106]
Methylenblau ist mutagen.[107][108][109][110] Im Tierversuch zeigte sich an Mäusen nach oraler Verabreichung von M.-Trihydrat an 5 d/Woche über 106 Wochen per Schlundsonde in Dosierungen von 2,5 bis 25 mg/kg KG x d eine dosisabhängige Zunahme von Adenomen und Karzinomen des Dünndarms; bei der höchsten Dosis lag die kombinierte Inzidenz von Adenomen und Karzinomen mit 12 % signifikant über der historischer Kontrollen.[111] Weiterhin wurde ein leichter Anstieg der Inzidenz bösartiger Lymphome beobachtet, der jedoch bei den Männchen nur marginal über der Inzidenz historischer Kontrollen lag und bei den Weibchen keine klare Dosisabhängigkeit zeigte; der Zusammenhang mit der Exposition wurde vom NTP daher als „nicht eindeutig“ („equivocal“) bewertet. Der Bewertung der US-amerikanischen Arzneimittelbehörde FDA zufolge weisen die Ergebnisse dieser Studie hingegen nicht auf eine substanzbedingte Entstehung von Tumoren bei Mäusen hin.[112] Bei Ratten zeigte sich nach entsprechender Verabreichung an 5 d/Woche über 106 Wochen per Schlundsonde in Dosierungen von 5 bis 50 mg M.-Trihydrat/kg KG x d bei den Männchen ein Trend für eine dosisabhängige Zunahme von Inselzelladenomen und möglicherweise von Adenomen + Karzinomen der Bauchspeicheldrüse. Bei Weibchen wurden keine erhöhte Inzidenz von Tumoren festgestellt. Das NTP sieht in diesen Befunden „einige Anzeichen“ („some evidence“) für eine kanzerogene Wirkung von Methylenblau bei männlichen und keine derartige Evidenz bei weiblichen Ratten. Die FDA kam zu dem Schluss, dass Methylenblau bei männlichen Ratten Inselzelladenome oder -karzinome der Bauchspeicheldrüse verursacht.
Gegenanzeigen
Methylenblau ist ein Monoaminoxidase-Hemmer (MAOI),[113] und kann bei intravenöser Verabreichung von Dosen über 5 mg/kg in Kombination mit selektiven Serotonin-Wiederaufnahmehemmern (SSRI) oder anderen Serotonin-Wiederaufnahme-Hemmern (z. B. Duloxetin, Sibutramin, Venlafaxin, Clomipramin, Imipramin, Fluoxetin, Fluvoxamin, Paroxetin, Sertralin und Citalopram) eine schwere Serotonin-Toxizität, das Serotoninsyndrom, auslösen.[114][115][116][117]
Es verursacht eine hämolytische Anämie bei Trägern des G6PD-Enzymmangels (Favismus) und sollte bei diesen nicht angewendet werden.[118][119] Ebenso sollte es nicht bei Patienten mit Heinz-Körper-Anämie verwendet werden.[106]
In der Schwangerschaft sollte Methylenblau aufgrund fruchtschädigender Wirkung nicht bei der Amniozentese angewendet werden.[120]
Aufnahme, Stoffwechsel und Ausscheidung
Die maximale Konzentration des Methylenblaus im Blutplasma wird bei intravenöser Gabe nach 0,5 Stunden und oral nach 2,2 Stunden erreicht.[121] Daher wird Methylenblau bei Methämoglobinämie intravenös verabreicht. Die Konzentration im Blut ist vier bis fünfmal höher als im Plasma, vermutlich weil es von Zellen aufgenommen wird.[9] Die orale Bioverfügbarkeit liegt bei etwa 72 %.[121] Die Fläche unter der Kurve von oral verabreichtem Methylenblau ist in Ratten nur 6,5 % derjenigen von intravenös verabreichtem, vermutlich aufgrund metabolischer Eigenheiten der Ratte.[122] Unter reduzierenden Bedingungen wie im Blut wird Methylenblau nach und nach zum Leukomethylenblau reduziert. Etwa 65 – 85 % des Methylenblaus wird in Zellen zum farblosen Leukomethylenblau reduziert.[9] In Ratten reichert sich Methylenblau nach der Aufnahme im Gehirn, in der Leber und in der Galle an.[122] Methylenblau wird in der Leber durch Cytochrom P450 verstoffwechselt und daneben über die Niere in den Urin ausgeschieden, weshalb Menschen mit geschädigter Leber oder Niere ein höheres Risiko für Methylenblau-Toxizität oder -Arzneimittelwechselwirkungen haben.[81] Da Methylenblau in der Galle angereichert wird, erfolgt auch eine Ausscheidung über den Darm.[9] Nach intravenöser Gabe werden in Ratten in 24 Stunden 28 % der Dosis über den Urin ausgeschieden, nach oraler Einnahme 18 % der Dosis in 24 Stunden.[122] Die biologische Halbwertszeit von Methylenblau nach intravenöser Gabe liegt für Menschen bei 5–24 Stunden.[57][122][121]
Literatur
- Ulrich L. Bohne, Richard P. Kreher: Methylenblau. Geschichte eines Farbstoffs – ein Farbstoff mit Geschichte. In: NiU-Chemie. Nr. 52, 1999, S. 36–37.
- R. H. Howland: Methylene Blue: The Long and Winding Road from Stain to Brain: Part 1. In: Journal of psychosocial nursing and mental health services. Band 54, Nummer 9, September 2016, S. 21–24, doi:10.3928/02793695-20160818-01, PMID 27576224.
- R. H. Howland: Methylene Blue: The Long and Winding Road From Stain to Brain: Part 2. In: Journal of psychosocial nursing and mental health services. Band 54, Nummer 10, Oktober 2016, S. 21–26, doi:10.3928/02793695-20160920-04, PMID 27699422.






