Hexahelicen
chemische Verbindung
From Wikipedia, the free encyclopedia
Hexahelicen ist ein polycyclischer aromatischer Kohlenwasserstoff aus der Gruppe der Helicene.

| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
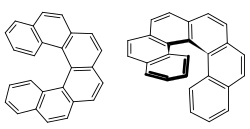 | ||||||||||
| (+)-Hexahelicen | ||||||||||
| Allgemeines | ||||||||||
| Name | Hexahelicen | |||||||||
| Summenformel | C26H16 | |||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 328,4 g·mol−1 | |||||||||
| Aggregatzustand |
fest[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Geschichte
Zum ersten Mal wurde Hexahelicen 1956 von Melvin und Lednicer in einer zehnstufigen Synthese ausgehend von Naphthalin-1-carbaldehyd synthetisiert. Damals wurden auch schon die Chiralität der Verbindung und ihre Racematspaltung beschrieben.[4][5]
Synthese
Hexahelicen sowie verschiedene substituierte Derivate können über Biphenyl-Naphthalin-Intermediate synthetisiert werden. Zunächst werden durch Sonogashira-Kupplungen und Suzuki-Kupplungen zwei Vorläufermoleküle hergestellt. Diese werden durch eine mit Pd(PPh3)4 katalysierte Suzuki-Kupplung verbunden und dann durch Platin(II)-chlorid zu Hexahelicen cyclisiert.[6]
Die Synthese gelingt auch ausgehend von 2,7-Dimethylnaphthalin in zwei Stufen mit einer Gesamtausbeute von 53 %. Dabei wird zunächst durch eine Siegrist-Kondensation mit Benzylidenanilin 2,7-Distyrylnaphthalin gebildet und dieses dann photocyclisiert. Da hierdurch ein teilweise gesättigtes Produkt entsteht wird für die Oxidation zu Hexahelicen elementares Iod zugesetzt.[7]
Eine teilweise enantioselektive Synthese von Hexahelicen ist durch eine Cyclisierung mittels zirkular polarisiertem Licht möglich. Geeignete Edukte sind 1-(2-Naphthyl)-2-(3-phenanthryl)ethylen (25 % Ausbeute) oder 1-(2-Benzo[c]phenanthryl)-2-phenylethylen (85 % Ausbeute). Als Intermediat entstehen dabei teilweise gesättigte Verbindungen, die aber durch Zusatz von elementarem Iod zum Reaktionsgemisch direkt in Hexahelicen überführt werden können.[8]
Resolution des Racemats
Racemisches Hexahelicen kann in seine beiden Enantiomere aufgetrennt werden, indem eines mittels enantiomerenreiner 2-(2,4,5,7-Tetranitrofluoriden-9-ylaminooxy)propansäure selektiv kristallisiert wird.[4][9]
Eigenschaften

Hexahelicen existiert in Form zweier Enantiomere. (−)-Hexahelicen entspricht einer linksdrehenden Helix und ist auch optisch linksdrehend. Demgegenüber entspricht (+)-Hexahelicen einer rechtsdrehenden Helix und ist optisch rechtsdrehend.[5] Bei höheren Temperaturen racemisiert enantiomerenreines Hexahelicen. Die Halbwertszeit wurde bei 187,6 °C zu 187 Minuten bestimmt, bei 205,2 °C zu 48 Minuten und bei 221,4 °C zu 13,4 Minuten.[10]
Racemisches Hexahelicen kristallisiert in der chiralen Raumgruppe P212121. Dabei liegt eine Schichtstruktur vor, bei der sich abwechselnde Schichten jeweils nur ein Enantiomer enthalten.[2][11] Hexahelicen weist Fluoreszenz auf.[12]
Hexahelicen bildet einen Komplex mit Silber(I), der sowohl in der Festphase (als Perchlorat) existiert als auch in der Gasphase.[13]
Toxizität
Die Umwelttoxizität von Hexahelicen wurde an verschiedenen Wasser- und Bodenorganismen untersucht. Bei den Wasserorganismen (Daphnia magna, Desmodesmus subspicatus und Vibrio fisheri) wurden keine relevanten toxikologischen Effekte detektiert. Für die Bodenorganismen Enchytraeus crypticus (Familie Enchytraeidae) und Folsomia candida war es hingegen giftig.[14]
Verwendung
Enantiomerenreine Helicene eignen sich als chirale Auxiliare.[15] Hexahelicen kann konkret für die enantioselektive Addition von Diisopropylzink an 2-(2-tert-Butylethinyl)pyrimidin-5-carbaldehyd verwendet werden.[16]
