Lithiumchromat
chemische Verbindung
From Wikipedia, the free encyclopedia
Lithiumchromat ist das Lithiumsalz der Chromsäure. Es ist ein starkes Oxidationsmittel und wie alle Chromate toxisch und krebserregend.

| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
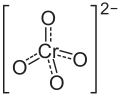 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Lithiumchromat | ||||||||||||||||||
| Summenformel | Li2CrO4 | ||||||||||||||||||
| Kurzbeschreibung |
gelbe geruchlose Kristalle[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 129,87 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,15 g·cm−3 (Dihydrat)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
gut in Wasser (48,6 g·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Darstellung
Lithiumchromat kann aus Lithiumcarbonat und Chromsäure hergestellt werden.[4][5]
Eigenschaften
Das Dihydrat kristallisiert im orthorhombischen Kristallsystem in der Raumgruppe P212121 (Raumgruppen-Nr. 19) mit den Gitterkonstanten a = 774,6 pm, b = 1201 pm und c = 550,9 pm sowie vier Formeleinheiten pro Elementarzelle.[6][7]
Das Anhydrat kristallisiert in der Phenakit-Struktur trigonal in der Raumgruppe R3 (Raumgruppen-Nr. 148) mit den Gitterparametern a = 14,01 Å und c = 9,41 Å sowie 18 Formeleinheiten pro Elementarzelle.[8]
Versetzt man Lithiumchromat mit Salpetersäure, so entsteht Lithiumdichromat.[5]
Beim Glühen mit Lithiumoxid bildet sich Lithiumchromat(V) Li3CrO4.[9][10]
Verwendung
Eine wässrige Lösung von Lithiumchromat wird als Korrosionsinhibitor sowie als Additiv in Batterien verwendet. Das Dihydrat wird daneben auch als Oxidationsmittel eingesetzt.[1]




