Mycomycin
chemische Verbindung
From Wikipedia, the free encyclopedia
Mycomycin ist ein natürlich vorkommendes Antibiotikum. Es ist eine stark ungesättigte Carbonsäure, welche zwei konjugierte Doppelbindungen und zwei konjugierte Dreifachbindungen aufweist. Zudem enthält sie zwei kumulierte Doppelbindungen; es handelt sich demnach um ein Allen. Sie zählt außerdem zu den Eninen, Diinen und Polyenen, sowie Alken- und Alkinsäuren.

| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
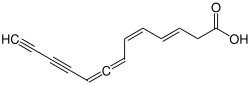 | |||||||||||||
| Unspezifizierte Stereochemie | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Mycomycin | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C13H10O2 | ||||||||||||
| Kurzbeschreibung |
farblose Nadeln[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 198,22 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Schmelzpunkt |
75 °C (explosionsartige Zersetzung)[2] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Vorkommen
Eigenschaften
Mycomycin ist ein Antibiotikum, das gegen Mycobacterium tuberculosis und verschiedene pathogene Pilze wirkt. Die Verbindung ist sehr instabil und zersetzt sich schnell, wenn sie nicht sehr kalt (z. B. auf Trockeneis) oder als verdünnte Lösung unter Inertgas gelagert wird. Bei Erhitzen in einer abgeschmolzenen Kapillare unter Stickstoff zersetzt es sich bei 75 °C explosionsartig.[2] Durch seine Allen-Substruktur ist es chiral und optisch aktiv (linksdrehend), mit einem Drehwinkel von .[1] Das Zentralatom im Allen trennt auch die beiden konjugierten Mehrfachbindungssysteme voneinander, was Einfluss auf die spektroskopischen Eigenschaften hat.[2][1]
Reaktionen
Durch Reaktion mit verdünntem Kaliumhydroxid bei 27 °C lagert sich Mycomycin zu Isomycomycin um.[1] Dabei kommt es zu einer Isomerisierung der Allenstruktur zu einer Dreifachbindung, zu einer Verschiebung der schon vorhandenen Dreifachbindungen und zu einer Isomerisierung der Z-Doppelbindung zu einer E-Doppelbindung.[2] Die Isomerisierung funktioniert analog auch mit Lithiumhydroxid oder Natriumhydroxid.[5]
Durch Umsetzung mit Kaliumpermanganat oder Natriumdichromat entsteht ein schwarzes polymeres Harz. Hydrierung ergibt Tridecansäure.[2]

![{\displaystyle \left[\alpha \right]_{\text{D}}^{25}=-130^{\circ }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/5af59339cf4241246c612442ac43b08b058c05a7)