Perchlorylfluorid
chemische Verbindung
From Wikipedia, the free encyclopedia
Perchlorylfluorid (FClO3) ist ein farbloses, giftiges Gas mit unangenehmem Geruch, welches leicht kondensierbar ist (Siedepunkt ca. −47 °C). Chemisch ist es das Säurefluorid der Perchlorsäure. Das Chlor liegt in seiner höchsten Oxidationsstufe +VII vor.

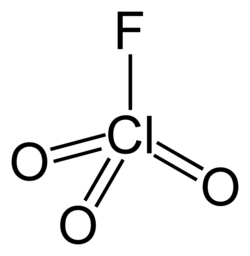
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Perchlorylfluorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | ClFO3 | ||||||||||||||||||
| Kurzbeschreibung |
farbloses Gas mit süßlichem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 102,45 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
gasförmig[1] | ||||||||||||||||||
| Dichte |
1,39 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
−46,8 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
schlecht in Wasser (0,6 g·l−1)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 3 ml·m−3 bzw. 13 mg·m−3[2] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Herstellung
Perchlorylfluorid kann durch Fluorierung von Kaliumchlorat mit Fluor in Antimonpentafluorid bei −20 °C[5] oder durch Umsetzung von Kaliumperchlorat mit Fluorsulfonsäure erhalten werden[5][6]:
Ebenfalls möglich ist die Umsetzung von Kaliumperchlorat mit Fluorwasserstoff und Antimon(V)-fluorid[7]:
Eigenschaften
Perchlorylfluorid ist bis über 400 °C beständig[5][8]. Es wirkt stark brandfördernd (oxidierend) und reagiert, v. a. beim Erhitzen, heftig mit Reduktionsmitteln. Auch viele Beschichtungsmittel, Kunststoffe und Gummi werden angegriffen. Mit Wasser reagiert es nur träge, abhängig vom pH-Wert, zu Perchlor- und Flusssäure.
Die Verbindung eignet sich zur Synthese von (zumeist explosionsfähigen) organischen Derivaten der Perchlorsäure. So können damit durch Reaktion mit Alkoholaten Perchlorsäureester hergestellt werden; mit Phenyllithium (C6H5Li) erhält man Perchlorylbenzol C6H5ClO3[9]. Mit reinem Natriummethylat erfolgt die Reaktion explosionsartig.[8] Mit Ammoniak und Aminen können sich Perchlorylamide R(R')N-ClO3 bilden, die bei unsubstituierten NH-Bindungen sauer wirken.[5]
Sicherheitshinweise
Bei Meerschweinchen führte die inhalative Gabe von 220 mg·m−3 Perchlorylfluorid zur Fibrose von Bindegewebe in der Lunge und Chronisch obstruktiver Lungenerkrankung sowie Verminderung der Anzahl von Erythrocyten und Erzeugung von Methämoglobin im Blut.[3]
Bei der Durchführung chemischer Reaktionen mit Perchlorylfluorid kam es in der Vergangenheit wiederholt zu unvorhergesehen Explosionen.[10]



![{\displaystyle {\mathrm {KClO} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}\mathrm {HSO} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {F} {}\mathrel {\longrightarrow } {}\mathrm {ClO} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {F} {}+{}\mathrm {KHSO} {\vphantom {A}}_{\smash[{t}]{4}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/9feb0ec50871ec8e3d2ba9dde10856b2bffa36f4)
![{\displaystyle {\mathrm {KClO} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}2\,\mathrm {HF} {}+{}\mathrm {SbF} {\vphantom {A}}_{\smash[{t}]{5}}{}\mathrel {\longrightarrow } {}\mathrm {ClO} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {F} {}+{}\mathrm {KSbF} {\vphantom {A}}_{\smash[{t}]{6}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/eaee9a568adefe01579918b54723dc06f54206ec)