Rubidiumoxalat
chemische Verbindung
From Wikipedia, the free encyclopedia
Rubidiumoxalat ist das Rubidiumsalz der Oxalsäure.
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
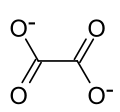 | |||||||
| Allgemeines | |||||||
| Name | Rubidiumoxalat | ||||||
| Summenformel | Rb2C2O4 | ||||||
| Kurzbeschreibung |
farblose, glanzlose Kristalle[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | |||||||
| Aggregatzustand |
fest | ||||||
| Dichte |
2,76 g·cm−3[1] (Monohydrat) | ||||||
| Schmelzpunkt |
Zersetzung[2] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||
Herstellung
Rubidiumoxalat kann aus Rubidiumcarbonat und Oxalsäure hergestellt werden.[5]
Es entsteht auch bei der thermischen Zersetzung von Rubidiumformiat.[6]
Eigenschaften
Rubidiumoxalat kristallisiert als Monohydrat (COO)2Rb2 im monoklinen Kristallsystem.[1] und ist isomorph zum Kaliumoxalat-Monohydrat.[7] Vom Anhydrat existieren bei Raumtemperatur zwei Modifikationen: Eine Modifikation ist monoklin und isotyp zu Caesiumoxalat, die andere ist orthorhombisch und isotyp zum Kaliumoxalat.[8] Frisch hergestelltes wasserfreies Rubidiumoxalat enthält zunächst hauptsächlich die monokline Phase, diese wandelt sich jedoch langsam irreversibel in die orthorhombische Modifikation um.[2] 2004 wurden zwei weitere Hochtemperaturphasen von Rubidiumoxalat entdeckt.[9]
Kristalldaten der verschiedenen Modifikationen von Rubidiumoxalat:
Die Standardbildungsenthalpie des kristallinen Rubidiumoxalates beträgt 1325,0 ± 8,1 kJ/mol.[11]
Die Zersetzung von Rubidiumoxalat unter Freisetzung von Kohlenmonoxid sowie in weiterer Folge Kohlendioxid und Sauerstoff findet bei 507–527 °C statt.[2][6]
Neben dem neutralen Rubidiumoxalat existiert auch ein Hydrogenoxalat mit der Formel RbH(COO)2, das isomorph zu entsprechenden Kaliumverbindung ist[12] und monokline Kristalle bildet,[13] sowie ein saures Tetraoxalat mit der Formel RbH3(COO)4, das als Dihydrat kristallisiert, bei 18 °C eine Dichte von 2,125 g/cm3 und bei 21 °C eine Löslichkeit von 21 g/l besitzt.[14]
Rubidiumoxalat bildet beim Eindampfen einer Lösung in Wasserstoffperoxid ein Monoperhydrat der Zusammensetzung (COO)2Rb2·H2O2, das monokline Kristalle bildet, die an der Luft relativ stabil sind.[15]
Mit Fluorwasserstoff reagiert Rubidiumoxalat unter Bildung einer Komplexverbindung.[16]






