User:Double sharp/Magnesium
Chemical element with atomic number 12 (Mg)
From Wikipedia, the free encyclopedia
 | ||||||||||||||||||||||||||
| Magnesium | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pronunciation | /mæɡˈniːziəm/ ⓘ | |||||||||||||||||||||||||
| Appearance | shiny grey solid | |||||||||||||||||||||||||
| Standard atomic weight Ar°(Mg) | ||||||||||||||||||||||||||
| Magnesium in the periodic table | ||||||||||||||||||||||||||
| Atomic number (Z) | 12 | |||||||||||||||||||||||||
| Group | group 2 (alkaline earth metals) | |||||||||||||||||||||||||
| Period | period 3 | |||||||||||||||||||||||||
| Block | s-block | |||||||||||||||||||||||||
| Electron configuration | [Ne] 3s2 | |||||||||||||||||||||||||
| Electrons per shell | 2, 8, 2 | |||||||||||||||||||||||||
| Physical properties | ||||||||||||||||||||||||||
| Phase at STP | solid | |||||||||||||||||||||||||
| Melting point | 923 K (650 °C, 1202 °F) | |||||||||||||||||||||||||
| Boiling point | 1363 K (1091 °C, 1994 °F) | |||||||||||||||||||||||||
| Density (at 20° C) | 1.737 g/cm3[3] | |||||||||||||||||||||||||
| when liquid (at m.p.) | 1.584 g/cm3 | |||||||||||||||||||||||||
| Heat of fusion | 8.48 kJ/mol | |||||||||||||||||||||||||
| Heat of vaporization | 128 kJ/mol | |||||||||||||||||||||||||
| Molar heat capacity | 24.869 J/(mol·K) [4] | |||||||||||||||||||||||||
| Specific heat capacity | 1023.205 J/(kg·K) [5] | |||||||||||||||||||||||||
Vapor pressure
| ||||||||||||||||||||||||||
| Atomic properties | ||||||||||||||||||||||||||
| Oxidation states | common: +2 0,[6] +1[7] | |||||||||||||||||||||||||
| Electronegativity | Pauling scale: 1.31 | |||||||||||||||||||||||||
| Ionization energies |
| |||||||||||||||||||||||||
| Atomic radius | empirical: 160 pm | |||||||||||||||||||||||||
| Covalent radius | 141±7 pm | |||||||||||||||||||||||||
| Van der Waals radius | 173 pm | |||||||||||||||||||||||||
| Other properties | ||||||||||||||||||||||||||
| Natural occurrence | primordial | |||||||||||||||||||||||||
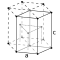
| Crystal structure | hexagonal close-packed (hcp) (hP2) | |||||||||||||||||||||||||
| Lattice constants | a = 320.91 pm c = 521.03 pm (at 20 °C)[3] | |||||||||||||||||||||||||
| Thermal expansion | 25.91×10−6/K (at 20 °C)[3][a] | |||||||||||||||||||||||||
| Thermal conductivity | 156[8] W/(m⋅K) | |||||||||||||||||||||||||
| Electrical resistivity | 43.9[9] nΩ⋅m (at 20 °C) | |||||||||||||||||||||||||
| Magnetic ordering | paramagnetic | |||||||||||||||||||||||||
| Molar magnetic susceptibility | +13.1×10−6 cm3/mol (298 K)[10] | |||||||||||||||||||||||||
| Young's modulus | 45 GPa | |||||||||||||||||||||||||
| Shear modulus | 17 GPa | |||||||||||||||||||||||||
| Bulk modulus | 35.4[11] GPa | |||||||||||||||||||||||||
| Speed of sound thin rod | 4940 m/s (at r.t.) (annealed) | |||||||||||||||||||||||||
| Poisson ratio | 0.290 | |||||||||||||||||||||||||
| Mohs hardness | 1–2.5 | |||||||||||||||||||||||||
| Brinell hardness | 44–260 MPa | |||||||||||||||||||||||||
| CAS Number | 7439-95-4 | |||||||||||||||||||||||||
| History | ||||||||||||||||||||||||||
| Naming | after Magnesia, Greece[12] | |||||||||||||||||||||||||
| Discovery | Joseph Black (1755[12]) | |||||||||||||||||||||||||
| First isolation | Humphry Davy (1808[12]) | |||||||||||||||||||||||||
| Isotopes of magnesium | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
- Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. (2022-05-04). "Standard atomic weights of the elements 2021 (IUPAC Technical Report)". Pure and Applied Chemistry. doi:10.1515/pac-2019-0603. ISSN 1365-3075.
- Arblaster, John W. (2018). Selected Values of the Crystallographic Properties of Elements. Materials Park, Ohio: ASM International. ISBN 978-1-62708-155-9.
- Rumble, p. 4.61
- Rumble, p. 4.61
- Mg(0) has been synthesized in a compound containing a Na2Mg22+ cluster coordinated to a bulky organic ligand; see Rösch, B.; Gentner, T. X.; Eyselein, J.; Langer, J.; Elsen, H.; Li, W.; Harder, S. (2021). "Strongly reducing magnesium(0) complexes". Nature. 592 (7856): 717–721. Bibcode:2021Natur.592..717R. doi:10.1038/s41586-021-03401-w. PMID 33911274. S2CID 233447380
- Bernath, P. F.; Black, J. H. & Brault, J. W. (1985). "The spectrum of magnesium hydride" (PDF). Astrophysical Journal. 298: 375. Bibcode:1985ApJ...298..375B. doi:10.1086/163620.. See also Low valent magnesium compounds.
- Rumble, p. 12.137
- Rumble, p. 12.28
- Rumble, p. 4.70
- Gschneider, K. A. (1964). Physical Properties and Interrelationships of Metallic and Semimetallic Elements. Solid State Physics. Vol. 16. p. 308. doi:10.1016/S0081-1947(08)60518-4. OCLC 646775097.
- Rumble, p. 4.19
- Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). "The NUBASE2020 evaluation of nuclear properties" (PDF). Chinese Physics C. 45 (3) 030001. doi:10.1088/1674-1137/abddae.
- The thermal expansion is anisotropic: the parameters (at 20 °C) for each crystal axis are αa = 25.31×10−6/K, αc = 27.03×10−6/K, and αaverage = αV/3 = 25.91×10−6/K.[3]