Difenilcetena
From Wikipedia, the free encyclopedia
| Difenilcetena | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| 2,2-difeniletenona | ||
| General | ||
| Fórmula molecular | C14H10O | |
| Identificadores | ||
| Número CAS | 525-06-4[1] | |
| ChemSpider | 109691 | |
| PubChem | 123069 | |
| UNII | 50BG2854L0 | |
| Propiedades físicas | ||
| Apariencia | Líquido oleoso anaranjado | |
| Masa molar | 194,233 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
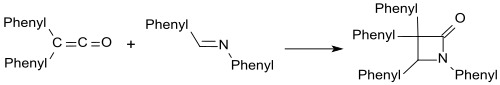
La difenilcetena es una sustancia química de la familia de las cetenas. La difenilcetena, como la mayoría de las cetenas disustituidas estables, es un aceite de color rojo anaranjado a temperatura y presión ambiente. Debido a los dobles enlaces sucesivos en la estructura de la cetena R1R2C=C=O, la difenil cetena es un heterocumuleno. La reacción más importante de la difenilcetena es la cicloadición [2+2] a enlaces múltiples C=C, C=N, C=O y C=S.[2]
La difenil cetena fue aislada por primera vez por Hermann Staudinger en 1905 e identificada como el primer ejemplo de la clase excepcionalmente reactiva de cetenos[3] con la fórmula general R1R2C=C=O (R1=R2=grupo fenilo).[4]
Preparación
La primera síntesis de H. Staudinger se basó en el uso de cloruro de 2-clorodifenilacetilo (preparado a partir de ácido bencílico y cloruro de tionilo[5]) del que se escinden dos átomos de cloro utilizando zinc en una reacción de deshalogenación:[3]

Una de las primeras síntesis descritas parte de bencilmonohidrazona (a partir de difeniletanodiona e hidrato de hidrazina[6]), que se oxida con óxido de mercurio (II) y sulfato de calcio para formar mono-diazocetona, y luego se convierte en difenilceteno a 100 °C bajo eliminación de nitrógeno con un rendimiento del 58%:

Otra de las primeras síntesis conocidas de la difenilcetena, la describió Eduard Wedekind, quien ya había obtenido difenilcetena en 1901 mediante la deshidrohalogenación de cloruro de difenilacetilo con trietilamina, sin embargo sin aislamiento ni caracterización.[7] Esta variante también fue descrita en 1911 por H. Staudinger.[8]

Un protocolo de laboratorio estándar se basa en el método de Staudinger y produce difenilcetena como un aceite naranja con rendimientos del 53-57%. En un proceso más reciente, el bromuro de 2-bromo-2,2-difenilacetilo se hace reaccionar con trifenilfosfina para producir difenilcetena con rendimientos de hasta el 81 %.[9]

Recientemente, se ha informado de una síntesis de difenilcetena a partir de ácido difenilacético y el reactivo de Hendrickson (anhídrido de trifenilfosfonio-trifluorometanosulfonato)[10] con eliminación de agua con un rendimiento del 72%.[11]


2CO-O-CO-{}}}{\text{Z-Leu }}{\ce {->[{} \atop {\ce {H-Phe-OEt}}]}}{\text{ Z-Leu}}{\ce {-Phe-OEt}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a7b4b915bc917b7c77143009ead9cc799bd83acc)