Galactoquinasa
From Wikipedia, the free encyclopedia
externos
| Galactocinasa 1[1] | ||||
|---|---|---|---|---|
 Figura 1. Modelo de cintas de un monómero de la galactocinasa 1 humana unida a la galactosa (en rojo) y a un análogo del ATP (en naranja). La esfera verde representa un ion de magnesio. | ||||
| Estructuras disponibles | ||||
| PDB | ||||
| Identificadores | ||||
| Nomenclatura |
Otros nombres Galactosa cinasa
| |||
| Símbolo | GALK1 (HGNC: 4118) | |||
| Identificadores externos |
Bases de datos de enzimas
| |||
| Número EC | 2.7.1.6 | |||
| Locus | Cr. 17 q23-q25 | |||
| Estructura/Función proteica | ||||
| Tamaño | 392 (aminoácidos) | |||
| Ortólogos | ||||
| Especies |
| |||
| Entrez |
| |||
| UniProt |
| |||
| RefSeq (ARNm) |
| |||
| PubMed (Búsqueda) |
| |||
| PMC (Búsqueda) |
| |||
| N-acetilgalactosamina cinasa[2] | ||||
|---|---|---|---|---|
| Estructuras disponibles | ||||
| PDB | Buscar ortólogos: PDBe, RCSB | |||
| Identificadores | ||||
| Nomenclatura |
Otros nombres Galactosa cinasa 2
| |||
| Símbolo | GALK2 (HGNC: 4119) | |||
| Identificadores externos | ||||
| Locus | Cr. 15 | |||
| Estructura/Función proteica | ||||
| Tamaño | 458 (aminoácidos) | |||
| Ortólogos | ||||
| Especies |
| |||
| Entrez |
| |||
| UniProt |
| |||
| RefSeq (ARNm) |
| |||
La galactocinasa (EC 2.7.1.6) es una enzima fosfotransferasa que cataliza la fosforilación de la D-galactosa a D-galactosa-1-fosfato utilizando ATP como donante del grupo fosfato.[3]
- D-galactosa + ATP α-D-galactosa-1-fosfato + ADP
La galactocinasa cataliza la primera etapa de la ruta de Leloir, una ruta metabólica encontrada en muchos organismos para el catabolismo de la β-D-galactosa a glucosa-1-fosfato.[4] La galactocinasa que fue aislada por primera vez del hígado de mamíferos, ha sido estudiada extensivamente en las levaduras,[5][6] arqueas,[7] plantas[8][9] y humanos.[10][11]
En el ser humano existen dos genes que codifican galactocinasas.
- El gen GALK1 codifica la galactocinasa 1.
- El gen GALK2 codifica la N-acetilgalactosamina cinasa. Esta enzima actúa como una galactocinasa cuando la galactosa está presente en altas concentraciones. De hecho se la conoce también como galactocinasa 2.[12]
Estructura

La galactocinasa está compuesta por dos dominios separados por un gran hueco. Las dos regiones son conocidas como los dominios N- y C-terminal. El anillo adenina del ATP se une en un agujero hidrofóbico localizado en la interfaz entre los dos dominios. El dominio N-terminal está compuesto por 5 filamentos formados de láminas beta y 5 hélices alfa. El dominio C-terminal está caracterizado por dos capas de láminas beta antiparalelas y 6 hélices alfa.[10] La galactocinasa no pertenece a la familia de las cinasas que actúan sobre carbohidratos, pero sí a la superfamilia de enzimas dependientes del ATP conocida como superfamilia GHMP cinasas.[14] GHMP es una abreviatura referente a los miembros originales de la familia: galactocinasa, homoserina cinasa, mevalonato cinasa y fosfomevalonato cinasa. Los miembros pertenecientes a la superfamilia GHMP tienen una gran similitud en su estructura tridimensional aunque solamente comparten entre un 10% y un 20% de su secuencia. Estas enzimas contienen tres motivos bien conservados (I, II y III), el segundo participa en la unión del nucleótido y tiene la secuencia Pro-X-X-X-Gly-Leu-X-Ser-Ser-Ala.[13]
Especificidad
En diferentes especies, las galactocinasas presentan una gran variedad de especificidad de sustrato.
- La galactocinasa de la Escherichia coli puede fosforilar 2-deoxi-D-galactosa, 2-amino-deoxi-D-galactosa, 3-deoxi-D-galactosa y fucosa. La enzima no puede tolerar ninguna modificación en el carbono 4 (C-4) de la galactosa, pero los cambios en el C-2 no interfieren con la función de la enzima.[15]
- Las galactocinasas de los humanos y ratas también son capaces de fosforilar la 2-deoxi-D-galactosa.[16][17]
- Contrariamente la galactocinasa de la Saccharomyces cerevisiae es altamente específica por la D-galactosa y no puede fosforilar glucosa, manosa, arabinosa, fucosa, lactosa, galactitol o 2-deoxi-D-galactosa.[5][6]
Por otra parte, las propiedades cinéticas de la galactocinasa también difieren en las diferentes especies.[10]
Mecanismo
Recientemente se han aclarado los roles de los aminoácidos del sitio activo de la galactocinasa humana. El Asp-186 extrae un protón del C1-OH de la α-D-galactosa y el alcóxido nucleófilo resultante ataca el γ-fosfato del ATP. Un grupo fosfato es transferido al azúcar y el Asp-186 es deprotonado por agua. El residuo cercano Arg-37 estabiliza a Asp-186 en su forma aniónica y se ha probado que es esencial para la función de la galactocinasa mediante experimentos de mutaciones puntuales.[11] Los residuos Asp y Arg del sitio activo están altamente conservado en las galactocinasas.[10]

Función biológica
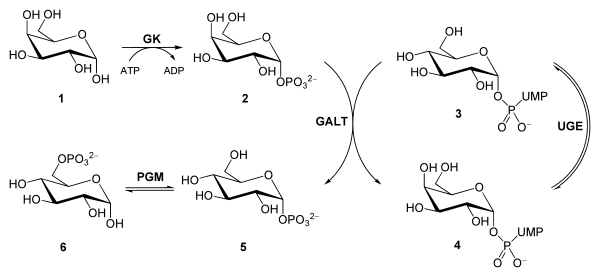
La ruta de Leloir cataliza la conversión de galactosa en glucosa. La galactosa se encuentra en los productos lácteos, frutas y vegetales, y puede ser producida de forma endógena por la rotura de las glicoproteínas y glicolípidos. En la ruta de Leloir participan tres enzimas: galactocinasa, galactosa-1-fosfato uridiltransferasa y UDP-galactosa 4-epimerasa. La galactocinasa cataliza la primera etapa del metabolismo de la galactosa formando galactosa-1-fosfato.[4][18]