Hantaviridae
familia de virus
From Wikipedia, the free encyclopedia
Orthohantavirus es un género de virus que incluye todos los hantavirus (familia Hantaviridae) capaces de causar enfermedad en humanos, (pero que no se transmiten entre personas). Los ortohantavirus, denominados en adelante hantavirus, se encuentran de forma natural principalmente en roedores (zoonosis). En general, cada hantavirus es portado por una sola especie de roedor, y cada roedor portador alberga una única especie de hantavirus. En sus reservorios naturales, los hantavirus suelen provocar una infección persistente y asintomática. Sin embargo, en humanos producen dos tipos de enfermedades: la fiebre hemorrágica con síndrome renal (FHSR) y el síndrome pulmonar por hantavirus (SPH o SPHV). La FHSR está causada principalmente por hantavirus de África, Asia y Europa —denominados hantavirus del Viejo Mundo—, mientras que el SPH es producido habitualmente por hantavirus de las Américas, conocidos como hantavirus del Nuevo Mundo.

| Hantavirus | ||
|---|---|---|
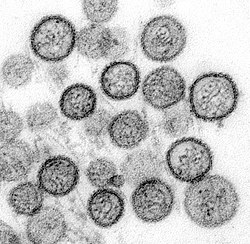 Imagen de microscopio electrónico de un tipo de Hantavirus | ||
| Taxonomía | ||
| Dominio: | Riboviria | |
| Reino: | Orthornavirae | |
| Filo: | Negarnaviricota | |
| Subfilo: | Polyploviricotina | |
| Clase: | Bunyaviricetes | |
| Orden: | Elliovirales | |
| Familia: | Hantaviridae | |
| Clasificación de Baltimore | ||
| Grupo: | V (Virus ARN monocatenario negativo) | |
Los hantavirus se transmiten principalmente a través de aerosoles y gotículas que contienen excreciones de roedores, así como por alimentos contaminados, mordeduras y arañazos. Factores ambientales como las precipitaciones, la temperatura y la humedad influyen en la transmisión. La FHSR se caracteriza por afección renal con inflamación de los riñones, exceso de proteínas en la orina (proteinuria) y sangre en la orina (hematuria). La tasa de letalidad de la FHSR oscila entre menos del 1% y el 15% según el virus. Una forma leve de FHSR, denominada nefropatía epidémica, suele estar causada por el virus Puumala y el virus Dobrava-Belgrado. El SPH presenta síntomas iniciales similares a los de la gripe —fiebre, cefalea y dolor muscular—, seguidos de insuficiencia respiratoria súbita. La tasa de letalidad del SPH es mayor que la de la FHSR, situada entre el 30 y el 60 %. En ambas enfermedades, la afección resulta del aumento de la permeabilidad vascular, la disminución del recuento de plaquetas y una respuesta exagerada del sistema inmunitario.
El genoma de los hantavirus consta de tres segmentos de ARN de sentido negativo monocatenario que codifican una proteína cada uno: una ARN polimerasa dependiente de ARN (RdRp), un precursor de glucoproteína de superficie y la proteína N. Los segmentos están encapsulados en proteínas N para formar complejos ribonucleoproteicos (RNP), cada uno de los cuales tiene una copia de la RdRp asociada. Los complejos RNP están rodeados por una envoltura lipídica de la que sobresalen las proteínas de espícula. La replicación comienza cuando las espículas se unen a la superficie celular. Tras la entrada en la célula, la envoltura se fusiona con endosomas y lisosomas, liberando los RNPs al citoplasma. La RdRp transcribe entonces el genoma para producir ARN mensajero (ARNm), que es traducido por los ribosomas del huésped para producir proteínas virales, y replica el genoma para los virus descendientes. Los hantavirus del Viejo Mundo se ensamblan en el aparato de Golgi y obtienen su envoltura de él antes de ser transportados a la membrana celular para salir mediante exocitosis. Los hantavirus del Nuevo Mundo se ensamblan cerca de la membrana celular y adquieren su envoltura al salir por gemación desde su superficie.
Los hantavirus fueron descubiertos tras la guerra de Corea. Durante el conflicto, la FHSR afectó con frecuencia a soldados apostados cerca del río Hantan. En 1978, en Corea del Sur, se aisló el primer hantavirus, el virus Hantaan, y se demostró que era el responsable del brote ocurrido durante la guerra. En pocos años se descubrieron otros hantavirus causantes de FHSR en toda Eurasia. En 1982, la Organización Mundial de la Salud dio nombre oficial a la FHSR, y en 1987 los hantavirus fueron clasificados por primera vez. El nombre del grupo deriva del virus Hantaan y del río Hantan. En 1993, un brote de SPH ocurrió en la región de las Cuatro Esquinas de los Estados Unidos, lo que llevó al descubrimiento de los hantavirus patógenos del Nuevo Mundo y de la segunda enfermedad causada por estos virus. Desde entonces, los hantavirus han sido hallados no solo en roedores, sino también en topos, musarañas y murciélagos.
Nomenclatura
El nombre Hantavirus —y por extensión Orthohantavirus— proviene del río Hantan, al norte de las ciudades coreanas de Dongducheon y Paju, cerca de donde se aisló el virus prototipo del grupo, el virus Hantaan. Es frecuente la confusión entre «Hantavirus» y «virus Hantaan». En castellano se comete a menudo el error de denominar «virus Hanta» a cualquier hantavirus, expresión que no existe como tal. Lo que sí existe es el «virus Hantaan» (HTNV), la especie tipo del género, que es la que le da nombre al conjunto. Siguiendo las reglas de nomenclatura taxonómica, el nombre del taxón debe presentarse en cursiva. Se considera un virus de riesgo de bioseguridad n.º 4.
Morfología
Los hantavirus tienen forma oval a esférica, con un diámetro de entre 70 y 350 nm. Son virus con envoltura que presentan en su interior una nucleocápsida helicoidal.[1] El genoma de los hantavirus es de ARN monocatenario, circular y de polaridad negativa, dividido en tres segmentos de diferente longitud: S, M y L. El segmento S (del inglés small, 'pequeño'), de alrededor de 2,1 kb, codifica la proteína N de la nucleocápsida, que se une al ARN viral y lo protege, y en algunos ortohantavirus también codifica la proteína no estructural NS, que inhibe la producción de interferón en las células del huésped. El segmento M (medium, 'medio'), de aproximadamente 3,7 kb, codifica un precursor de glucoproteína que se cotraduce y escinde en las glucoproteínas Gn y Gc, las cuales se unen a los receptores celulares, regulan las respuestas inmunitarias e inducen anticuerpos protectores. El segmento L (large, 'grande'), de aproximadamente 6,6 kb, codifica la ARN polimerasa dependiente de ARN (RdRp), que media la transcripción y la replicación del ARN viral. Cada virión presenta tres nucleocápsidas; cada una está conformada por uno de los tres segmentos de ARN (S, M o L) y copias de la proteína N. Serológicamente, la proteína N se emplea para detectar las variantes específicas del virus. La envoltura viral tiene su origen en las membranas de las células infectadas y presenta las proteínas Gn y Gc que protruyen de su superficie e intervienen en la adhesión viral a las células diana. Los hantavirus no codifican proteínas de matriz que ayuden a estructurar el virión, por lo que aún se desconoce cómo las proteínas de superficie se organizan en una esfera con un enrejado simétrico.[2]
Taxonomía
Nomenclatura
Esta familia toma su denominación de los primeros casos en orillas del río Hantaan, en Corea; el virus responsable era el Virus Hantaan.
Es frecuente la confusión entre "Hantavirus" y "Virus Hantaan". Por un error de traducción, se hace entender al grupo biológico "Hantavirus" como "virus Hanta", cosa que no existe. Lo que si existe es el "Virus Hantaan" (o HTNV), la especie tipo del género Hantavirus y la que le da el nombre al grupo. Es común encontrar este tipo de error en la literatura castellana, muchas veces expresado con no concordancia de número, considerando "Hantavirus" como un sustantivo singular o haciendo mención de un "virus Hanta" cuando corresponde la denominación genérica "Hantavirus". También, respetando las reglas de nomenclatura taxonómica, lo correcto es que este taxón esté presentado en itálica (que es lo usual).
Hantavirus
La siguiente es una lista alfabética de especies de virus incluidas en la familia de Hantaviridae. Entre paréntesis constan las siglas usuales para la denominación viral.
- Virus Andes (ANDV)
- Virus Bayou (BAYV)
- Virus Black Creek Canal (BCCV)
- Virus Cano Delgadito (CADV)
- Virus Choclo (CHOV)
- Virus Dobrava-Belgrade (DOBV)
- Virus El Moro Canyon (ELMCV)
- Virus Hantaan (HTNV)
- Virus Isla Vista (ISLAV)
- Virus Khabarovsk (KHAV)
- Virus Laguna Negra (LANV)
- Virus Muleshoe (MULx)
- Virus New York (NYV)
- Virus Prospect Hill (PHV)
- Virus Puumala (PUUV)
- Virus Rio Mamore (RIOMV)
- Virus Rio Segundo (RIOSV)
- Virus Seoul (SEOV)
- Virus Sin Nombre (SNV)
- Virus Thailand (THAIV)
- Virus Thottapalayam (TPMV)
- Virus Topografov (TOPV)
- Virus Tula (TULV)
- Virus que infectan a la subfamilia Murinae
- Hantaan, HTN, Apodemus agrarius, Corea, Asia y Europa, FHSRb Sí
- Seoul SEO Rattus norvegicus, R. rattus, Corea Asia, Europa, América FHSR Sí
- Dobrava-Belgrade DOB Apodemus flavicollis, Eslovenia, Europa, Oriente Medio FHSR Sí
- Thai-749 THAI Bandicota indica, Tailandia, Asia, Se desconoce Sí
- Virus que infectan a la subfamilia Arvicolinae
- Puumala PUU Clethrionomys glareolus, Finlandia, Europa, Asia, FHSR Sí
- Prospect Hill PH Microtus pennsylvanicus, Maryland, América del Norte, Se desconoce Sí
- Tula TUL Microtus arvalis, Rusia, Europa, Se desconoce Sí
- Jabárovsk KBR Microtus fortis, Rusia, Asia, Se desconoce Sí
- Topografov TOP Lemmus sibiricus, Siberia Rusia, Asia, Se desconoce Sí
- Isla Vista ISLA Microtus californicus, California, América del Norte, Se desconoce No
- Virus que infectan a la subfamilia Sigmodontinae
- Sin Nombre SN Peromyscus maniculatus, Nuevo México, América del Norte, SPHc Sí
- New York NY Peromyscus leucopus, Nueva York, América del Norte, SPH Sí
- Black Creek Canal BCC Sigmodon hispidus, Florida, América, SPH Sí
- Bayou BAY Oryzomys palustris, Luisiana, Sudeste de los Estados Unidos, SPH Sí
- Caño Delgadito CANO Sigmodon alstoni, Venezuela, América del Sur, Se desconoce Sí
- Río Mamore RM Oligoryzomys microtis, Bolivia, América del Sur, Se desconoce Sí
- Laguna Negra CHP Calomys laucha, Paraguay, América del Sur, SPH Sí
- Muleshoe MULE Sigmodon hispidus, Texas, América, Se desconoce No
- El Moro Canyon ELMC Reithrodontomys megalotis, California, América del Norte, Se desconoce No
- Río Segundo RIOS Reithrodontomys mexicanus, Costa Rica, México, América Central, Se desconoce No
- Andes AND Oligoryzomys longicaudatus, Argentina, América del Sur, SPH Sí
- Virus que infectan a insectívoros
- Thottapalayam TPM Suncus murinus, India, Asia, Se desconoce Sí
Clínica y filogenia
El análisis filogenético de los genes de los Hantavirus transmitidos por roedores ha indicado la existencia de tres linajes principales. Los virus que causan FHSR pertenecen a un linaje del Viejo Mundo, en tanto que los virus que causan SPHV comparten un linaje común del Nuevo Mundo y están en miembros de una sola subfamilia de roedores (Sigmodontinae) de la familia Muridae.
Algunos de los virus presentes en roedores sigmodontinos constituyen especies independientes, según pruebas genéticas, serológicas, vínculo con el huésped reservorio o los tres tipos de pruebas. Otros virus están en proceso de evaluación, igual que los criterios para definir los Hantavirus spp.
En el continente americano se han identificado trece Hantavirus spp. y, de ellos, seis causan SPHV. Los anticuerpos séricos de pacientes de SPHV muestran reacción cruzada intensa con otros virus del Nuevo Mundo, pero en grado variable con los antígenos de Hantavirus spp. del Viejo Mundo.
Se reconocen dos grupos de Hantavirus spp. que se asocian a dos presentaciones clínicas diferentes: los Hantavirus del Viejo Mundo y los del Nuevo Mundo (Vignoli et al.).
Los Hantavirus del Viejo Mundo son predominantes en Asia (sobre todo en China y Corea) y Europa (Alemania, Francia, Bélgica, Holanda y Rusia); incluyen las especies Hantaan, Puumala, Seoul, Prospect Hill y Dobrava. Estos producen un cuadro conocido como fiebre hemorrágica con síndrome renal (FHSR) y son responsables de 100 000 casos anuales, presentando una mortalidad que oscila entre el 1 y 15% (Vignoli et al.).
Los Hantavirus del Nuevo Mundo predominan en toda América. Se identifican como productores de enfermedad febril asociada con insuficiencia respiratoria aguda, shock y una mortalidad del 60 a 80%; esta forma clínica se conoce como síndrome pulmonar por Hantavirus (SPHV).
Tras el brote en la región de Cuatro Esquinas (Four Corners, al sudoeste de EE. UU.) en 1993, fue identificado por primera vez un Hantavirus en el continente americano. Fue denominado "Virus Sin Nombre", "Convict Creek" o "Muerto Canyon", que hoy se conoce con el nombre de Four Corners (FC). Otro en el Nuevo Mundo es el Virus Andes, identificado en 1995, produjo la epidemia de SPHV en El Bolsón y Lago Puelo (Argentina) en 1996, aportando por primera vez evidencia epidemiológica de contagio persona a persona, ocasión en que fueron infectados varios médicos, algunos con desenlace fatal.
Infecciones por Hantavirus
La infección por Hantavirus genera dos cuadros clínicos diferentes: la fiebre hemorrágica con síndrome renal (FHSR); y el síndrome pulmonar por hantavirus (SPHV).
El SPHV está producido por el Virus Sin Nombre, pero otros virus también están involucrados. Se han identificado cuatro Hantavirus como responsables de FHSR con síndrome renal:
- Virus Hantaan: transmitido por ratones de campo (Apodemus agrarius);
- Virus Seoul: transmitido por ratas (Rattus rattus y R. norvegicus);
- Virus Puumala: transmitido por varios roedores silvestres;
- Virus Dobrava: transmitido por otras especies de ratones de campo.
Hantavirus spp. son importantes en el ambiente de investigación clínico-científico, pues es común que estos virus se encuentren como contaminantes potenciales de materiales de laboratorio[3], de las muestras de animales para experimentación (se dispone de roedores) y sus derivados (anticuerpos monoclonales, cultivos celulares, etc).
Prevención
La prevención más efectiva es eliminar o minimizar el contacto con roedores.[4]
Como el virus es transmitido por saliva, excreciones y mordeduras de roedores la protección en áreas comunes es clave para la prevención de la enfermedad.
Una prevención general se logra evitando lugares donde puedan alojarse y reproducirse roedores. Por eso es importante desechar nidos, sellar agujeros, colocar trampas vivas, limpiar y desinfectar con frecuencia, evitar dejar alimento de fácil acceso para roedores (migas, comida en el suelo, etc.).[5]
Es importante tener consideraciones particulares en industrias u hogares en zonas rurales, así como personas en riesgo como menores o adultos mayores (jardines, escuelas, geriátricos, etc). En caso de visualizar roedores se debe comunicar a entes gubernamentales de control de plagas como áreas de zoonosis, es común que los Estados tengan áreas específicas. A su vez existen diversas guías para diversos sectores que permiten que la ciudadanía adopte medidas para la reducción de los riesgos, tal es el caso del Manual para el Control Integral de Roedores (Colombia)[6] y el Manual para el control de roedores en el ámbito domiciliario (INTA).[7]
Tratamiento
Dado que las opciones de tratamiento son limitadas, la mejor protección es evitar los roedores y sus hábitats.
Científicos de la Universidad de Concepción (Chile), liderados por María Inés Barría, descubrieron el primer tratamiento específico, con base en anticuerpos monoclonales. El proceso comenzó con detectar por qué algunos pacientes sobrevivían al virus y se encontró que tenían una gran cantidad de anticuerpos neutralizantes.[8]
En Chile, según protocolos del Ministerio de Salud, un paciente con infección por Hantavirus suele ser intubado, sometido a ventilación mecánica y, si comienzan a deteriorarse sus signos vitales, suele aplicársele un protocolo de oxigenación por membrana extracorpórea (ECMO), tratamiento que implica oxigenar la sangre fuera del cuerpo y luego reintroducirla.
Otra indicación autorizada por el Minsal desde 2016 es la transfusión de plasma convalesciente, es decir, plasma inmune de pacientes que sobrevivieron a la infección y que se presume han desarrollado anticuerpos.
En Argentina, se registró en 2024 un estudio de uso compasivo con tocilizumab (inhibidor del receptor de interleucina-6) para el síndrome cardiopulmonar por hantavirus grave, diseñado como estudio antes-y-después; al 20 de agosto de 2025 el estudio continúa activo y sus resultados aún no han sido evaluados por pares.[9]
Epidemiología
América del Norte
Canadá
La causa principal de la enfermedad en Canadá son los ratones ciervos infectados con el virus Sin Nombre. Entre 1989 y 2014, hubo un total de 109 casos confirmados, con una tasa de mortalidad estimada del 29 %. El virus existe en ratones ciervos en todo el país, pero los casos se concentraron en el oeste de Canadá (Columbia Británica, Alberta, Saskatchewan y Manitoba), con solo un caso en el este del país. Aproximadamente el 70 % de los casos se han asociado con actividades domésticas y agrícolas en entornos rurales.
Estados Unidos
Hasta enero de 2017, se habían notificado 728 casos de hantavirus en los Estados Unidos desde 1995, en 36 estados. Más del 96 % de los casos han ocurrido al oeste del río Misisipi. Los estados con mayor número de casos son Nuevo México (109), Colorado (104), Arizona (78), California (61) y Washington (50), entre otros. El 36 % del total de casos notificados han resultado en muerte.
América del Sur
Los agentes del SPH identificados en América del Sur incluyen el virus Andes —el único hantavirus del que existe evidencia de transmisión de persona a persona— y el virus Laguna Negra, pariente cercano del virus Río Mamoré. Los roedores que han demostrado portar hantavirus en la región incluyen Abrothrix longipilis y Oligoryzomys longicaudatus.
El virus Andes fue identificado en 1995 y provocó una epidemia de SPH en El Bolsón y Lago Puelo (Argentina) en 1996, aportando por primera vez evidencia epidemiológica de contagio entre personas, ocasión en que fueron infectados varios médicos, algunos con desenlace fatal.
En 2026 se produjo un brote en el crucero Hondius que dejó varios infectados y al menos 3 fallecidos.[10][11]
Asia
En China, la península de Corea y Rusia, la FHSR está causada principalmente por los virus Hantaan, Puumala y Seúl. En marzo de 2020, un hombre de Yunnan (China) dio positivo por hantavirus y falleció mientras viajaba a Shandong; según los informes de Global Times, alrededor de otras 32 personas fueron analizadas para detectar el virus en ese momento.
Europa
En Europa se conocen principalmente dos hantavirus causantes de FHSR: el virus Puumala y el virus Dobrava-Belgrado. El virus Puumala es portado por el topillo rojo (Clethrionomys glareolus) y está presente en la mayor parte de Europa, excepto en la región mediterránea. Generalmente provoca una enfermedad relativamente leve denominada nefropatía epidémica, que se manifiesta con fiebre, cefalea, síntomas gastrointestinales, insuficiencia renal y visión borrosa. Las infecciones por virus Dobrava son similares, pero a menudo incluyen también complicaciones hemorrágicas.
El virus Dobrava-Belgrado presenta cuatro genotipos conocidos, cada uno portado por una especie de roedor diferente. Solo en 2017, el Instituto Robert Koch (RKI) de Alemania recibió 1.713 notificaciones de infecciones por hantavirus.
Bibliografía
- Organización Panamericana de la Salud (OPS): Hantavirus en las Américas: guía para el diagnóstico, el tratamiento, la prevención y el control. desarrollado por el Grupo Especial para el Estudio de Hantavirus, marzo de 1998, Georgia, EE. UU.
- Trilla García A & Alonso Fernández PL: Infecciones causadas por arbovirua y arenavirus: viriasis transmitidas por artrópodos y roedores, en Farreras Valentí P & Rozman C: Medicina Interna, (2)330:2857-2864, 14ª Harcourt, Madrid, 2000.
- Vignoli R, Calvelo E, Chiparelli H, Schelotto F: Virosis Emergentes de Importancia Regional: Virus Hanta, Dep.Bact.Vir., Fac.Med., Montevideo, Uruguay.
