Par de Lewis frustrado
From Wikipedia, the free encyclopedia
| Ácidos y Bases | |
|---|---|
 | |
| Ácidos y Bases | |
| |
| Tipos de ácidos | |
| Tipos de bases | |
En química, un par de Lewis frustrado (FLP por sus siglas en inglés) es un compuesto o mezcla que contiene un ácido de Lewis y una base de Lewis que, debido al impedimento estérico, no se puede combinar para formar un aducto clásico.[1] Se han ideado muchos tipos de FLP y muchos sustratos simples exhiben activación.[2][3]
El descubrimiento de que algunos FLP se dividieron en H2[4] desencadenó un rápido crecimiento de la investigación en FLPs. Debido a su reactividad "no extinguida", tales sistemas son reactivos hacia sustratos que pueden experimentar heterólisis. Por ejemplo, muchos FLPs dividen la molécula de hidrógeno. Por lo tanto, una mezcla de triciclohexilfosfina (PCy3) y tris (pentafluorofenil) borano reacciona con el hidrógeno para dar los iones de fosfonio y borato respectivos:
Esta reactividad se ha explotado para producir FLP que catalizan las reacciones de hidrogenación.[5]
Hidrógeno
Se ha demostrado que los pares de Lewis frustrados activan muchas moléculas pequeñas, ya sea por inducción de la heterólisis o por coordinación.
El descubrimiento de que algunos FLP pueden dividir y, por lo tanto, activar, H2[4] desencadenó un rápido crecimiento de la investigación en esta área. La activación y por lo tanto uso de H2 es importante para muchas transformaciones químicas y biológicas. El uso de FLP para liberar H2 no contiene metales, esto es beneficioso debido al costo y al suministro limitado de algunos metales de transición comúnmente utilizados para activar H2 (Ni, Pd, Pt).[6] Los sistemas FLP son reactivos frente a sustratos que pueden sufrir una heterólisis (por ejemplo, hidrógeno) debido a la reactividad "no apagada" de dichos sistemas. Por ejemplo, se ha demostrado anteriormente que una mezcla de triciclohexilfosfina (PCy3) y tris (pentafluorofenil) borano reacciona con H2 para dar los iones de fosfonio y borato respectivos:
En esta reacción, PCy3 (la base de Lewis) y B (C6F5)3 (el ácido de Lewis) no pueden formar un aducto debido al impedimento estérico de los grupos ciclohexilo y pentafluorofenilo voluminosos. El protón en el fósforo y el hidruro del borato ahora están "activados" y posteriormente pueden "entregarse" a un sustrato orgánico, dando como resultado la hidrogenación.
Mecanismo de activación del dihidrógeno por FLP
El mecanismo para la activación de H2 por FLP ha sido discutido, tanto para el intermolecular y casos intramoleculares. Los FLP intermoleculares son donde la Base de Lewis es una molécula separada del Ácido de Lewis, se piensa que estas moléculas individuales interactúan a través de las interacciones de la dispersión secundaria de Londres para unir la Base de Lewis y el Ácido (un efecto preorganizativo) donde las moléculas pequeñas pueden interactuar con los FLP. La evidencia experimental de este tipo de interacción a nivel molecular no está clara. Sin embargo, existe evidencia de apoyo para este tipo de interacción basada en estudios computacionales de DFT (Teoría de la Funcionalidad de la Densidad). Los FLP intramoleculares son donde el ácido de Lewis y la base de Lewis se combinan en una molécula mediante un enlazador covalente. A pesar de los "efectos preorganizativos" mejorados, se cree que los marcos rígidos de FLP intramoleculares tienen una reactividad reducida a las moléculas pequeñas debido a una reducción en la flexibilidad.
Ejemplo de activación de dihidrógeno
La activación de H2 mediante FLP se informó por primera vez en 2006.[4] En este informe se observó una especie de fosfonio-borato de someterse a la pérdida térmica de una molécula de H2, para generar la fosfina y el borano. La especie de borato de fosfonio 1 se preparó a partir de B(C6F5)3 y (C6H2Me3)2PH, debido a las exigencias estéricas de ambas moléculas, no se pudo formar un aducto tradicional y se preparó fosfato bipolar-boronato [Figura 1]. Se llevó a cabo un "intercambio de H por F" para obtener 2 que era estable a la humedad y al aire. Esta sal lanzará H molecular 2 cuando se calienta por encima de 100 °C, un cambio de color también se observó desde el incoloro 2 a la naranja-rojo 3 (tanto en THF). Esta reacción se invierte al reaccionar 3 con H2 a 25 °C, donde el cambio de color se invierte y 2 se reforma. La reacción de H2 con 3 fue un éxito para temperaturas tan bajas como 25 °C. La recristalización de 3 en THF proporcionó cristales incoloros del aducto 4 .

Otros sustratos de molécula pequeña
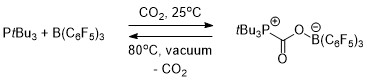
FLP también son reactivos frente a muchos sustratos insaturados más allá de H2. Algunos FLP reaccionan con el CO2, específicamente en la reducción desoxigenativa del CO2 al metano.[7]
El hecho de que los pares ácido-base se comporten de forma tanto nucleófila como electrófila al mismo tiempo ofrece un método para la apertura de anillos de éteres cíclicos como el THF, el 2,5-dihidrofurano, el cumarano y el dioxano.[8]
![{\displaystyle {\mathrm {PCy} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {B} (\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {F} {\vphantom {A}}_{\smash[{t}]{5}}){\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}[\mathrm {HPCy} {\vphantom {A}}_{\smash[{t}]{3}}]{\vphantom {A}}^{+}~[\mathrm {HB} (\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {F} {\vphantom {A}}_{\smash[{t}]{5}}){\vphantom {A}}_{\smash[{t}]{3}}]{\vphantom {A}}^{-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3c7ea46199d1f74478288c7affc7bdd1fc964071)
![{\displaystyle {\mathrm {PCy} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {B} (\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {F} {\vphantom {A}}_{\smash[{t}]{5}}){\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{4}}{}\mathrel {\longrightarrow } {}\mathrm {Cy} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {P} {\vphantom {A}}^{+}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {B} {\vphantom {A}}^{-}(\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {F} {\vphantom {A}}_{\smash[{t}]{5}}){\vphantom {A}}_{\smash[{t}]{3}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/08c2584242f41dac6a7dc67ea03d518339c29d81)