Monelline
From Wikipedia, the free encyclopedia
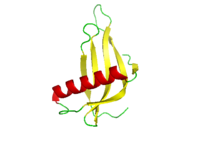
La monelline est une protéine au goût sucré, découverte dans le fruit du Dioscoreophyllum volkensii (en), un arbuste vivant en Afrique. La monelline est l'une des sept protéines connues qui sont naturellement édulcorantes : la brazzéine, la thaumatine, la lysozyme, la mabinline, la curculine (ou Néoculine) et la pentadine. Elle est de 800 à 2 000 fois plus sucrée que le sucre à poids égal, et résistante à la chaleur.
Découverte en 1969, la monelline fut d'abord considérée comme un carbohydrate[1].
En 1972, elle fut nommée d'après le Centre Monell des Sens Chimiques de Philadelphie, aux États-Unis, où elle fut isolée et caractérisée[2].
Source
La monelline est naturellement présente dans le fruit du Dioscoreophyllum volkensii, une plante grimpante dicotylédone tropical de la famille des Menispermaceaes. La plante est native de l'Afrique, on la trouve au Sierra Leone, en Érythrée, et au sud de l'Angola et du Mozambique. Elle est présente dans la forêt tropicale à basse altitude[3].